Literatuurreview
Literatuurconclusies stoppen met psychofarmaca voor probleemgedrag bij mensen met dementie
Effect van stoppen van antipsychotica op symptomen en terugval
Hoog GRADE | Conventionele en atypische antipsychotica kunnen gestopt worden zonder dat dit stoppen leidt tot toename van symptomen of tot terugval bij zes van de zeven gebruikers. |
Effect van stoppen van antidepressiva op symptomen en terugval
Matig GRADE | Tweede generatie antidepressiva kunnen gestopt worden zonder dat dit stoppen leidt tot toename van symptomen of tot terugval bij zes van de zeven gebruikers. |
Effect van stoppen van cholinesteraseremmers op symptomen en terugval
Laag GRADE | Cholinesteraseremmers kunnen worden gestopt bij patiënten met Alzheimer, Pick of FTD zonder dat dit leidt tot toename van symptomen. |
Literatuuronderzoek naar de effecten van stoppen van psychofarmaca voor probleemgedrag bij mensen met dementie
PICO:
P patiënten met dementie die langdurig psychofarmaca gebruiken vanwege probleemgedrag
I stoppen van het psychofarmacon (placebo)
C doorgaan met het psychofarmacon
O toename afname van symptomen, terugval (geen terugval), uitval
Bij stopstudies wordt effectiviteit vaak niet benoemd in termen van succesvol afbouwen (NNT), maar als toename van symptomen en percentage terugval (NNH). De kerngroep is ook geïnteresseerd in het percentage patiënten dat bij stoppen van een psychofarmacon vergeleken met doorgaan niet terugvalt.
Gevonden studies
Voor alle groepen van psychofarmaca (antipsychotica, antidepressiva, anti-epileptica, anxiolytica/ hypnotica/ melatonine, dementieremmers, cannabinoïden) is gezocht naar RCT’s en meta-analyses van RCT’s waarin onderzocht werd of deze psychofarmaca succesvol gestopt konden worden bij patiënten die deze middelen kregen in verband met probleemgedrag.
Er werden voor de antipsychotica twee meta-analyses en twaalf volledige artikelen van tien stopstudies beoordeeld. De volgende acht RCT’s voldeden aan de inclusiecriteria: Devanand 2011, Devanand 2012 (ADAD-studie), Ballard 2008/2009 (DART-AD-studie), Ruth 2008 (BEDNURS-studie), Ballard 2004, van Reekum 2002, Bridges-Parlet 1997 en Findlay 1989. De redenen om twee RCT’s te excluderen staan beschreven in bijlage 1. De meest recente meta-analyse van Pan (2014) was beperkt tot Engelstalige artikelen, maar deze meta-analyse, noch de eerdere meta-analyse van Declerq (2013) vonden extra RCT’s in andere talen. De kwaliteit van beide meta-analyses was voldoende en zij includeren dezelfde RCT’s, maar Declerq poolde minder resultaten dan Pan. De uitgebreide beschrijvingen van de RCT’s en de risico op bias beoordelingen van Declerq zijn gebruikt, alsmede de resultaten van Pan. Zo nodig zijn aanvullende gegevens verzameld en analyses gedaan.
Er werd één RCT over het stoppen van antidepressiva op volledige tekst beoordeeld en geschikt bevonden (Bergh, 2012). Voor het stoppen van cholinesteraseremmers werden de volledige teksten van één meta-analyse en acht RCT’s beoordeeld. Op twee RCT’s na (Holmes, 2004; Kertesz, 2008), betroffen deze studies het stoppen van dementieremmers bij patiënten met dementie die deze middelen niet voor de indicatie probleemgedrag hadden gekregen. Voor de anti-epileptica, anxiolytica/ hypnotica/ melatonine en cannabinoïden werden geen RCT’s geschikt bevonden.
De volgende studies voldeden aan de selectiecriteria:
1. Pan (2014) en Declerq (2013): dit zijn reviews van acht RCT’s waarin het stoppen van een antipsychoticum (abrupt of met een afbouwschema, en vervangen met placebo), dat oorspronkelijk gegeven was voor probleemgedrag bij mensen met dementie, vergeleken werd met het continueren van het antipsychoticum (in dezelfde dosis als de patiënt al gebruikte). De algemene studiekenmerken van deze acht RCT’s staan in tabel 1. De meetinstrumenten varieerden, maar vijf RCT’s hadden de NPI gebruikt. Een van de acht RCT’s scoorde een laag risico op bias (Ballard 2009). Alle studies werden verricht in Noord-Amerika of West-Europa.
2. Bergh (2012; DESEP-studie): dit betreft een Noorse antidepressivum stopstudie bij 128 verpleeghuispatiënten met Alzheimer of vasculaire dementie, die escitalopram, citalopram, sertraline, of paroxetine gedurende minstens drie maanden hadden gebruikt voor neuropsychiatrische symptomen maar niet voor depressie. Neuropsychiatrische symptomen werden gemeten met de NPI. De studie had een hoog risico op bias.
3. Holmes (2004) en Kertesz (2008): dit zijn twee cholinesteraseremmer stopstudies. In de RCT van Holmes (2004) werd het stoppen van donepezil (vervangen door placebo) vergeleken met doorgaan na twaalf weken gebruik. De patiënten hadden Alzheimerdementie en licht probleemgedrag (gemiddelde NPI-totaalscore was elf) ten tijde van de start van donepezil. In de RCT van Kertesz (2008) werd het stoppen van galantamine vergeleken met doorgaan bij patiënten met de ziekte van Pick of FTD na achttien weken gebruik. Gedragssymptomen van FTD werden gemeten met FBI, neuropsychiatrische symptomen in het algemeen met de NPI.
Tabel 1. Kenmerken en kwaliteit van geïncludeerde gerandomiseerde placebogecontroleerde stopstudies naar psychofarmaca voor probleemgedrag bij mensen met dementie
Studie | Medicijn | Stopsnelheid | Setting | Ernst, type dementi | Type Probleemgedrag | N | Trialduur, weken | Meetinstrument voor reductie symptomen | Kwaliteit van opzet en uitvoering1 |
Antipsychotica | |||||||||
Ballard 2004 | Conv. AP of risperidon >3 mnd. | abrupt | instelling | Licht-ernstig, AD | NG | 100 | 13 | NPI | 3/6 |
Ballard 2008/ 2009 | Conv. AP of risperidon > 3 mnd. | abrupt | instelling | Matig-ernstig, AD | BPSD | 165 | 24 | NPI | 5/6 |
Bridges-Parlet 1997 | Conv. AP >3 mnd. | Abrupt of tapering | instelling | Ernstig, vooralAD | Fysieke agressie | 36 | 4 | Aantal agressieve uitingen | 4/6 |
Devanand 2011 | Haloperidol ged 5 mnd., Responders* | tapering | thuis | Licht-ernstig, AD | Agitatie of psychose | 21 | 24 | BPRS | 2/6 |
Devanand 2012 | Risperidon ged 16 wkn. responders | tapering | instelling + thuis | Licht-ernstig, AD | Agitatie of psychose | 110 | 16 | NPI | 1/6 |
Findlay 1989 | Thioridazine >2 mnd. | tapering | instelling | Matig-ernstig, AD | divers probleemgedrag | 36 | 4 | SCAGS en LPRS | 2/6 |
Ruths 2008 | Haloperidololanzapine risperidon >3 mnd. | abrupt | instelling | NG, alle typen | BPSD | 55 | 4 | NPI-Q | 3/6 |
Van Reekum 2002 | Conv ap, risperidone, olazapine >6 mnd. | tapering | instelling | Matig-ernstig, alle typen | NG | 34 | 24 | Behave-AD, NPI | 2/6 |
Antidepressiva | |||||||||
Bergh 2012 | escitalopram, citalopram, sertraline, paroxetine >3 mnd. | tapering | instelling | Mild-ernstig AD, VAD, mixed | Diverse NPS (niet depressie) | 128 | 25 | NPI | 2/6 |
Dementieremmers | |||||||||
Holmes 2004 | Donezepil ged 12 wkn. | 10 mg | thuis | mild–matig AD | Diverse NPS | 96 | 6 | NPI | 3/6 |
Kertesz 2008 | Galantamine ged 18 wkn. | 16-24 mg | thuis | Pick/FTD (30-80) | Diverse NPS | 36 | 8 | FBI (primair), NPI | 4/6 |
AD: ziekte van Alzheimer; AQ: Aphasia Quotient of the Western Aphasia Battery; BPSD: behavioural or psychiatric disturbance; FBI Frontal Behavioral Inventory NG: niet gerapporteerd; LPRS = London Psychogeriatric Rating Scale; NPI-Q = Neuropsychiatric Inventory Questionnaire; SCAGS = Sandoz Clinical Assessment Geriatric Scale
* voor de trial gebruikten de patiënten diverse psychotrope medicatie en die werden gedurende één week afgebouwd alvorens ze haloperidol kregen gedurende vijf maanden.
$ latere follow-up metingen zijn niet meegenomen in de meta-analyse.
Resultaten en bewijskracht over effectiviteit
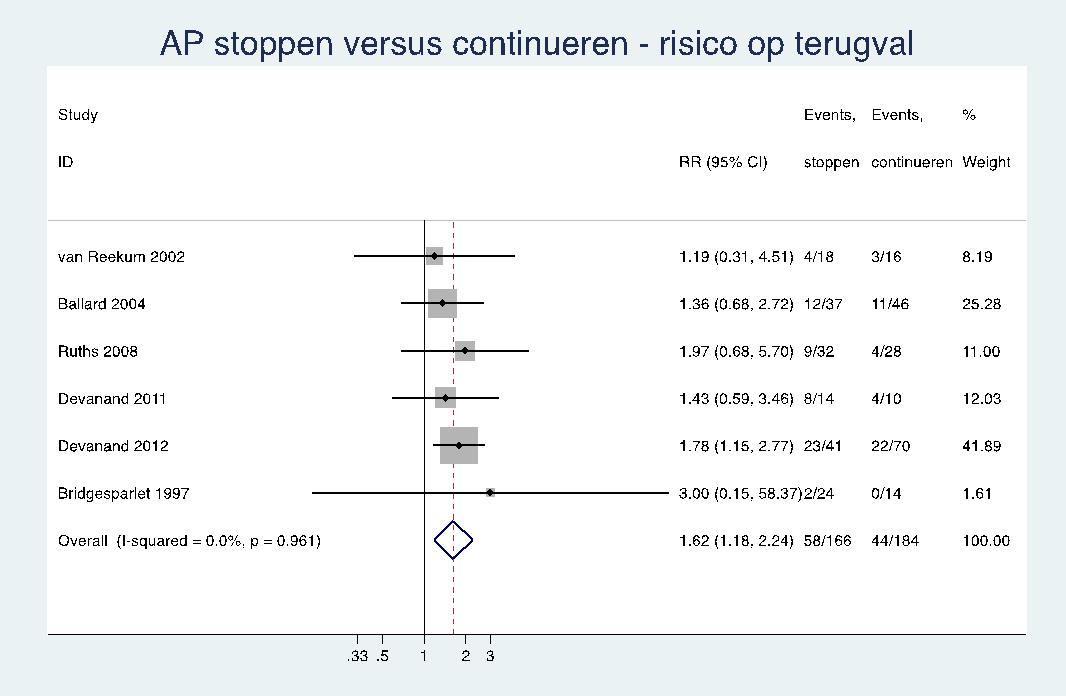
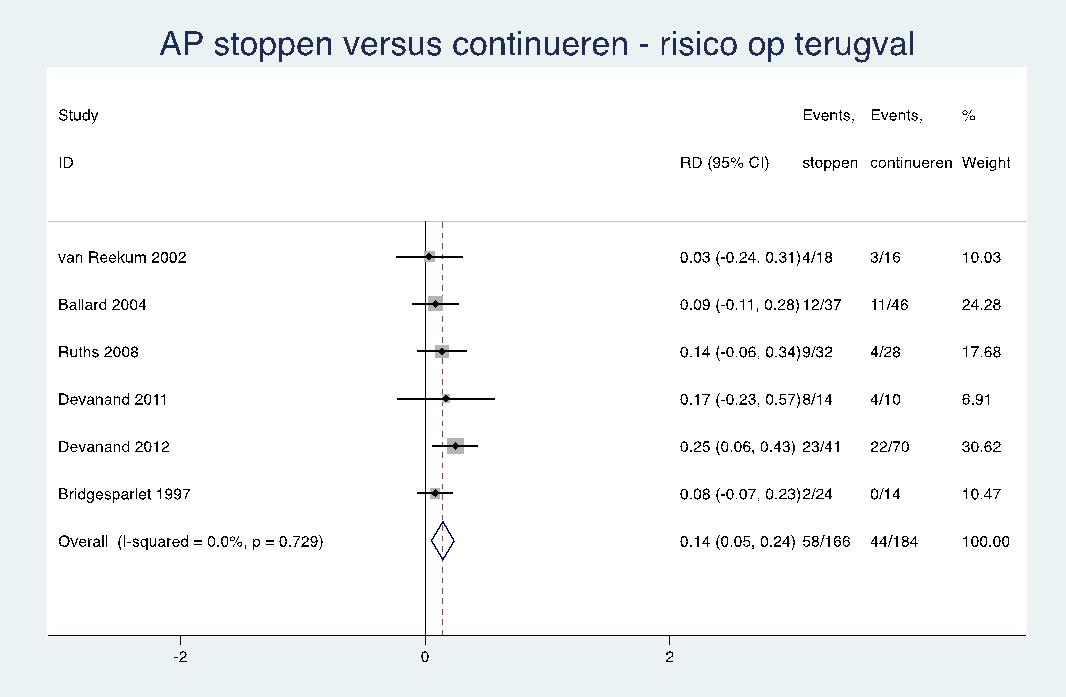
Tabel 2 toont het evidenceprofiel met details over de GRADE-beoordelingen. De forest plots zijn weergegeven in bijlage 3. De meta-analyse van Pan (2014) vond dat op het einde van de RCT’s het gemiddelde verschil in de ernst van het probleemgedrag in de groep die het antipsychoticumgebruik stopte, niet verschilde van die in de groep die doorging met het antipsychoticum (SMD= 0,19; 95% BI: –0,20 tot 0,58). Stoppen van een antipsychoticum leidde tot terugval (verslechtering van probleemgedrag) in 38% van de patiënten en doorgaan leidde tot terugval in 24% van de patiënten (RR= 1,62; 95% BI: 1,18 tot 2,24; ARR= 15%; 95% BI: 5% tot 23%). De NNH van stoppen is 7 (95% BI: 4 tot 20). Anders gezegd, bij zes van de zeven patiënten leidt stoppen van een antipsychoticum niet tot terugval. Ons vertrouwen in de kracht van het bewijs was hoog.
In de RCT van Bergh (2012) was de gemiddelde NPI-totaalscore klinisch niet maar statistisch wel significant verschillend na 25 weken stoppen van het antidepressivumgebruik versus doorgaan (SMD= 0,28; 95% BI: 0,06 tot 0,50). Stoppen van het antidepressivum leidde in 21% van de patiënten tot terugval, en doorgaan in 9% (OR= 2,7; 95% BI: 1,0 tot 7,3; ARR= 12%; 95% BI: -0% tot 24%). De NNH van stoppen is 7 (95% BI: 4 tot ∞). Kortom, bij zes op de zeven patiënten leidt stoppen niet tot terugval. De bewijskracht was matig vanwege het gebrek aan precisie.
In de donepezilstop (Holmes 2004), was de gemiddelde verandering in de NPI-totaalscore na zes weken stoppen, klinisch en statistisch verschillend (SMD= 0,49; 95% BI: 0,09 tot 0,88). Het percentage patiënten met terugval werd niet gerapporteerd. De bewijskracht is beoordeeld op laag vanwege het risico op (publicatie) bias en het gebrek aan precisie.
In de RCT van Kertesz (2008) leidde het stoppen met galantamine na acht weken eerder tot minder dan tot meer probleemgedrag in de groep die doorging versus stopte op zowel de FBI (SMD= -0,68; 95% BI: -1,36 tot -0,004) als NPI (SMD= 0,15; 95% BI: -0,20 tot 0,50). Maar het verschil was net wel respectievelijk niet statistisch significant. Het percentage patiënten dat terugviel werd niet gerapporteerd. De bewijskracht is beoordeeld op matig vanwege het gebrek aan precisie.
Resultaten en bewijskracht over uitval
De kans op uitval was niet verschillend tussen de groepen die stopten en doorgingen met antipsychoticum gebruik (OR= 1,11; 95% BI: 0,87 tot 1,41; ARR= 4%; 95% BI: -4% tot 12%) in de acht antipsychoticum stopstudies. Ons vertrouwen in de bewijskracht voor deze uitkomstmaat was hoog.
In de antidepressivum-stopstudie was het percentage uitval hoger en net statistisch significant in de groep die stopte versus de groep die doorging met gebruik (OR= 2,1; 95% BI: 1,0 tot 4,2; ARR= 17; 95% 0 tot 33%). De bewijskracht was laag vanwege risico op bias en gebrek aan precisie.
In de donepezil stopstudie was het verschil in uitval tussen de groep die stopte en de groep die doorging, klinisch en statistisch niet-significant verschillend (OR= 1,3; 95% BI: 0,4 tot 3,7; ARR= 3%; 95% BI: -12% tot 18%). De bewijskracht was laag vanwege risico op bias en gebrek aan precisie. In de galantamine-stopstudie was er geen verschil in uitval tussen de groepen (RR= 1,0; 95% BI: 0,1 tot 14,8; ARR= 0%; 95% BI: -15% tot 15%) in beide groepen. De bewijskracht is beoordeeld op matig vanwege gebrek aan precisie.
Tabel 2. Evidenceprofiel stopstudies psychofarmaca voor probleemgedrag bij mensen met dementie
| RCT’s (N) | Kwaliteit van het bewijs | n/N per groep* | Behandeleffecten van stoppen versus doorgaan | Algemene beoordeling | |||||
Vertekend1 | inconsistent | indirect | Niet precies2 | Publicatie bias | Stoppen (placebo) | Doorgaan | SMD/OR/ARR (95% BI) | |||
Antipsychoticum stoppen (diverse conventionele en atypische) | ||||||||||
Toename symptomen | 3$ | ja | nee | nee | nee | ja | 104/137 | 110/146 | SMD= 0,19 (–0,20 tot 0,58) | hoog |
Terugval | 6 | Ja, ten nadele van stoppen | nee | nee | nee | nee | 58/210 | 44/228 | RR= 1,62 (1,18 tot 2,24)^ ARR= 15% (5% tot 23%) | hoog |
Uitval | 8 | ja | nee | nee | ja | nee | 71/216 | 67/246 | RR= 1,11 (0,87; 1,41)^ ARR= 4% (-4% tot 12%) | laag |
Antidepressivum stoppen (diverse 2e generatie) | ||||||||||
Toename symptomen | 1 | ja | nee | nee | ja | ja | 35/63 | 46/68 | SMD= 0,28 (0,06 tot 0,50) | matig |
Terugval | 1 | ja | nee | nee | ja | ja | 13/63 | 6/68 | OR= 2,7 (1,0 tot 7,3) ARR=12% (-0% tot 24%) | matig |
Uitval | 1 | ja | nee | nee | ja | ja | 28/63 | 19/68 | OR= 2,1 (1,0 tot 4,2) ARR=17% (+0% tot 33%) | laag |
Cholinesteraseremmer stoppen (donepezil) | ||||||||||
Toename symptomen | 1 | ja | nee | nee | ja | ja | 55/55 | 41/41 | SMD= 0,49 (0,09 tot 0,88) | laag |
Terugval | 0 |
|
|
|
|
|
|
|
|
|
Uitval | 1 | ja | nee | nee | ja | ja | 10/55 | 6/41 | OR=1,3 (0,4 tot 3,7) ARR= 3% (-12% tot 18%) | laag |
Speciale vormen van dementie: Cholinesteraseremmer stoppen in patiënten met FTD (galantamine) | ||||||||||
Toename symptomen | 1 | ja | nee | nee | ja | nee | 17/18 | 17/18 | FBI: -0,68 (-1,36 tot -0,004) NPI: 0,15 (-0,20 tot 0,50) | matig |
Terugval | 0 |
|
|
|
|
|
|
|
|
|
Uitval | 1 | ja | nee | nee | ja | nee | 1/18 | 1/18 | RR =1,0 (0,1-14,8)# ARR=0% (-15% tot 15%) | matig |
Afkortingen: ARR= Absolute risicoreductie; BI= betrouwbaarheidsinterval; NS= niet significant; SMD= standardized mean difference.
$: Ballard, 2004; Ballard 2008/2009; Ruths, 2008
* betreft het aantal patiënten waarvan data gerapporteerd was voor berekening van SMD, het aantal patiënten dat terugviel, of dat uitviel.
^ RR in plaats van OR omdat het percentage terugvallers/ uitvallers boven de 30% lag.
# RR omdat 95% BI rondom OR niet geschat kon worden
Ballard CG, Thomas A, Fossey J, et al. (2004) A 3-month, randomized, placebo-controlled, neuroleptic discontinuation study in 100 people with dementia: the neuropsychiatric inventory median cutoff is a predictor of clinical outcome. J Clin Psychiatry;65(1):114-119.
Ballard C, Lana MM, Theodoulou M, et al. (2008) A randomised, blinded, placebo-controlled trial in dementia patients continuing or stopping neuroleptics (the DART-AD trial). PLoS Med ;5(4):e76.
Bergh S, Selbaek G, Engedal K. (2012) Discontinuation of antidepressants in people with dementia and neuropsychiatric symptoms (DESEP study): double blind, randomised, parallel group, placebo controlled trial. Bmj. 2012;344:e1566.
Bridges-Parlet S, Knopman D, Steffes S. Withdrawal of Neuroleptic Medications from Institutionalized Dementia Patients: Results of a Double-Blind, Baseline-Treatment-Controlled Pilot. Study.J Geriatr Psychiatry Neurol; 10:119-1126.
Declercq T, Petrovic M, Azermai M, et al. (2013) Withdrawal versus continuation of chronic antipsychotic drugs for behavioural and psychological symptoms in older people with dementia. Cochrane Database Syst Rev. 2013;3:Cd007726.
Devanand DP, Pelton GH, Cunqueiro K, et al. (2011) A 6-month, randomized, double-blind, placebo-controlled pilot discontinuation trial following response to haloperidol treatment of psychosis and agitation in Alzheimer’s disease. Int J Geriatr Psychiatry; 26(9):937-943.
Devanand DP, Mintzer J, Schultz SK, et al. (2012) Relapse risk after discontinuation of risperidone in Alzheimer’s disease. N Engl J Med;367(16):1497-1507.
Findlay DJ, Sharma J, McEwen J. (1989) Double-blind controlled withdrawal of thioridazine treatment in elderly female inpatients with senile dementia. Int J Ger Psychiatry; 4: 115-120.
Holmes C, Wilkinson D, Dean C, et al. The efficacy of donepezil in the treatment of neuropsychiatric symptoms in Alzheimer disease. Neurology. 2004;63(2):214-219.
Kertesz A, Morlog D, Light M, et al. Galantamine in frontotemporal dementia and primary progressive aphasia. Dement Geriatr Cogn Disord. 2008;25(2):178-185.
Pan YJ, Wu CS, Gau SS, Chan HY, Banerjee S. Antipsychotic discontinuation in patients with dementia: a systematic review and meta-analysis of published randomized controlled studies. Dement Geriatr Cogn Disord. 2014;37(3-4):125-40.
Van Reekum R, Clarke D, Conn D, et al. A randomized, placebo-controlled trial of the discontinuation of long-term antipsychotics in dementia. Int Psychogeriatr. 2002;14(2):197-210.
Ruths S, Straand J, Nygaard HA, Aarsland D. Stopping antipsychotic drug therapy in demented nursing home patients: a randomized, placebo-controlled study--the Bergen District Nursing Home Study (BEDNURS). Int J Geriatr Psychiatry. 2008;23(9):889-895.
Zuidema SU, Johansson A, Selbaek G, Murray M, Burns A, Ballard C, Koopmans RT. A consensus guideline for antipsychotic drug use for dementia in care homes. Bridging the gap between scientific evidence and clinical practice. Int Psychogeriatr. 2015 Nov;27(11):1849-1859.
En supplement: https://www.cambridge.org/core/journals/international-psychogeriatrics/article/consensus-guideline-for-antipsychotic-drug-use-for-dementia-in-care-homes-bridging-the-gap-between-scientific-evidence-and-clinical-practice/2EDA7ADF3E62D0358FA928029FFCB643#fndtn-supplementary-materialshttps://www.cambridge.org/core/journals/international-psychogeriatrics/article/consensus-guideline-for-antipsychotic-drug-use-for-dementia-in-care-homes-bridging-the-gap-between-scientific-evidence-and-clinical-practice/2EDA7ADF3E62D0358FA928029FFCB643#fndtn-supplementary-materials
Bijlage 1. Exclusietabel stopstudies psychofarmaca voor probleemgedrag bij mensen met dementie
Auteur en jaartal | Redenen van exclusie |
Ballard C, Thomas A, Gerry S, et al. A double-blind randomized placebo-controlled withdrawal trial comparing memantine and antipsychotics for the long-term treatment of function and neuropsychiatric symptoms in people with Alzheimer’s disease (MAIN-AD). J Am Med Dir Assoc. 2015;16(4):316-322. | In controle groep werd antipsychoticum vervangen door memantine (i.p.v. placebo) |
Cohen-Mansfield J, Lipson S, Werner P, et al. Withdrawal of haloperidol, thioridazine, and lorazepam in the nursing home: a controlled, double-blind study. Arch Intern Med. 1999 Aug 9-23;159(15):1733-40. | Antipsychoticum en lorazepam werden tegelijkertijd gestopt. |
Gaudig M, Richarz U, Han J, Van Baelen B, Schauble B. Effects of galantamine in Alzheimer’s disease: double-blind withdrawal studies evaluating sustained versus interrupted treatment. Curr Alzheimer Res. 2011;8(7):771-780. | Indicatie was Alzheimer dementie en galantamine gebruik van 3 of 5 maanden (geen probleemgedrag) |
Herrmann N, O’Regan J, Ruthirakuhan M, et al. A Randomized Placebo-Controlled Discontinuation Study of Cholinesterase Inhibitors in Institutionalized Patients With Moderate to Severe Alzheimer Disease. J Am Med Dir Assoc. 2016;17(2):142-147. | Indicatie was >2 jaar cholinesteraseremmer gebruik bij mensen met dementie (geen probleemgedrag) |
Howard R, McShane R, Lindesay J, et al. Donepezil and memantine for moderate-to-severe Alzheimer’s disease. N Engl J Med. 2012;366(10):893-903. | Indicatie was Alzheimer dementie en donepezil gebruik >3 maanden (geen probleemgedrag) |
Johannsen P, Salmon E, Hampel H, et al. Assessing therapeutic efficacy in a progressive disease: a study of donepezil in Alzheimer’s disease. CNS Drugs. 2006;20(4):311-325.
| Indicatie was Alzheimer dementie en twijfelachtig cognitief effect op donepezil gedurende 12-24 weken (geen probleemgedrag) |
Scarpini E, Bruno G, Zappala G, et al. Cessation versus continuation of galantamine treatment after 12 months of therapy in patients with Alzheimer’s disease: a randomized, double blind, placebo controlled withdrawal trial. J Alzheimers Dis. 2011;26(2):211-220. | Indicatie was Alzheimer dementie en galantamine gebruik >12 maanden (geen probleemgedrag) |
O’Regan J, Lanctot KL, Mazereeuw G, Herrmann N. Cholinesterase inhibitor discontinuation in patients with Alzheimer’s disease: a meta-analysis of randomized controlled trials. J Clin Psychiatry. 2015;76(11):e1424-31. | Meta-analyse van cholinesteraseremmer stopstudies maar RCT’s geïncludeerd die niet over probleemgedrag gaan. |
Bijlage 2. Risico op bias in stopstudies psychofarmaca voor probleemgedrag bij mensen met dementie *
Studie |
| 1. randomisatie proces | 2. afwijkingen van beoogde interventie | 3. ontbrekende metingen/ uitval | 4. geblindeerde metingen | 5. selectieve rapportage | 6. overig | aantal items zonder bias | |
| Antipsychotica | ||||||||
Ballard 2004 |
| Onduidelijk | Onduidelijk | Wel bias | Geen bias | Geen bias | geen bias | 3 | |
Ballard 2008/ 2009 |
| Geen bias | Onduidelijk | Geen bias | Geen bias | Geen bias | Geen bias | 5 | |
Bridges-Parlet 1997 |
| Onduidelijk | Geen bias | Onduidelijk | Geen bias | Geen bias | Geen bias | 4 | |
Devanand 2011 |
| Onduidelijk | Geen bias | wel bias | Geen bias | onduidelijk | Wel bias | 2 | |
Devanand 2012 |
| Wel bias | Onduidelijk | wel bias | Geen bias | Wel bias | Wel bias | 1 | |
Findlay 1989 |
| Wel bias | Geen bias | onduidelijk | Geen bias | Onduidelijk | Onduidelijk | 2 | |
Ruths 2008 |
| Onduidelijk | Onduidelijk | Onduidelijk | Geen bias | Geen bias | Geen bias | 3 | |
Van Reekum 2002 |
| Wel bias | Geen bias | wel bias | Geen bias | wel bias | Wel bias | 2 | |
| Antidepressiva stoppen | ||||||||
Bergh 2012 |
| wel bias | onduidelijk | wel bias | geen bias | wel bias | Wel bias | 2 | |
| Cholinesteraseremmer stoppen | ||||||||
Holmes 2004 |
| onduidelijk | Geen bias | Wel bias | Geen bias | Geen bias | Wel bias | 3 | |
Kertesz 2008 |
| Geen bias | onduidelijk | Geen bias | Geen bias | Geen bias | Wel bias | 4 | |
|
|
|
|
|
|
|
|
|
|
* zie tabblad ‘Verantwoording en methode’ voor uitleg over de risico op bias beoordeling
Bijlage 3. Forest plots stopstudies psychofarmaca voor probleemgedrag bij mensen met dementie