Literatuurconclusies
Literatuurconclusies psychosociale en psychologische interventies
Activiteitentherapie
Van de drie RCT’s die specifiek het effect van gespecificeerde activiteitentherapie (activiteiten gebaseerd op Montessori-methode; sensomotorische activiteiten) op geagiteerd gedrag bij verpleeghuisbewoners met dementie en geagiteerd gedrag onderzochten, vonden twee er een positief effect (Buettner, 1996; Lin, 2009) tijdens de therapie en één geen effect (Van der Ploeg, 2013).
|
Zeer laag GRADE |
Er zijn enige aanwijzingen voor afname van geagiteerd gedrag bij verpleeghuisbewoners met dementie tijdens specifieke op de persoon afgestemde activiteiten bij verpleeghuisbewoners. Er is geen specifieke activiteit die bij grote groepen cliënten gemiddeld duidelijk effectiever is in het verminderen van geagiteerd gedrag. |
Muziekinterventie
Van de negen RCT’s naar effect van muziektherapie op geagiteerd gedrag bij mensen met dementie en agitatie, vonden er zes een positief effect (Garland, 2007; Gerdner, 2000; Hicks-Moore, 2008; Remington, 2002; Ridder, 2013; Sung, 2006) tijdens of kort na de therapie en drie geen effect (Cooke, 2010; Groene, 1993; Vink, 2012).
|
Zeer laag GRADE |
Er zijn enige aanwijzingen voor een positief effect van een individuele niet specifiek op de persoon afgestemde muziekinterventie met rustige muziek op geagiteerd gedrag bij mensen met dementie, zowel tijdens als tot een uur na de interventie. |
|
Zeer laag GRADE |
Er zijn enige aanwijzingen voor een positief effect van een individuele op de persoon afgestemde muziekinterventie op geagiteerd gedrag bij mensen met dementie, zowel tijdens als tot een uur na de interventie. |
|
Zeer laag GRADE |
Er zijn enige aanwijzingen dat een individueel aangeboden muziekinterventie tot toename van dwaalgedrag kan leiden, zowel tijdens als tot een uur na de interventie. |
|
Zeer laag GRADE |
Er zijn geen aanwijzingen dat groepsgewijs aangeboden muziekinterventies een groter positief effect hebben op geagiteerd gedrag bij mensen met dementie in een instelling in vergelijking met andere recreatieve activiteiten. |
|
Zeer laag GRADE |
Er zijn enige aanwijzingen voor een positief effect van een groepsgewijs aangeboden muziekinterventie gecombineerd met bewegen op geagiteerd gedrag bij mensen met dementie in een zorginstelling. Het effect is geobserveerd tot een uur na afloop van de interventies. |
|
Zeer laag GRADE |
Er is geen aanwijzing dat het combineren van luisteren naar favoriete en/of rustige muziek met handmassage effectiever is voor het verminderen van agitatie, dan de afzonderlijke toepassing van muziekinterventie of handmassage. |
Zintuiglijke interventies
Van de acht RCT’s die zintuigelijke interventies onderzochten bij mensen met dementie en geagiteerd gedrag vonden er drie geen effect van massage (Baillon, 2004; Fu, 2013; Moyle, 2014) op geagiteerd gedrag. Vijf RCT’s vonden een positief effect voor acupressuur (Lin, 2009; Yang, 2015), handmassage (Hicks-Moore, 2008; Remington, 2002) en therapeutische aanraking (Hawranik, 2008) op geagiteerd gedrag.
|
Zeer lage GRADE |
Er zijn enige aanwijzingen dat zintuiglijke interventies als acupressuur, handmassage en therapeutische aanraking bij mensen met dementie en geagiteerd gedrag, geagiteerd gedrag kunnen verminderen. |
Aromatherapie
Van de zes RCT’s die aromatherapie bij mensen met dementie en geagiteerd gedrag onderzochten, vonden er vier (Fu, 2013; Lin, 2007; O’Connor, 2013; Yang, 2015) geen effect voor lavendel, één geen effect voor citroenmelisse (Burns, 2011) en één een positief effect voor citroenmelisse (Ballard, 2002).
|
Zeer lage GRADE |
Er zijn geen aanwijzingen dat aromatherapie met lavendelolie bij mensen met dementie en geagiteerd gedrag leidt tot vermindering van geagiteerd gedrag. |
|
Zeer lage GRADE |
Er zijn enige aanwijzingen dat aromatherapie met citroenmelisse bij mensen met dementie en geagiteerd gedrag tot afname van geagiteerd gedrag kan leiden. |
|
Zeer lage GRADE |
Er zijn geen aanwijzingen voor ernstige bijwerkingen van aromatherapie. |
Mediatieve cognitief gedragstherapeutische interventies
Er zijn vier RCT’s die het effect onderzochten van mediatieve cognitief gedragstherapeutische interventies bij mensen met dementie en geagiteerd gedrag die thuis verblijven. Drie RCT’s lieten geen effect zien (Gormley, 2001; Wright, 2001; Huang, 2003) en één RCT toonde op slechts één van de drie evaluatiemomenten een positief effect (Huang, 2013).
Er zijn vijf RCT’s die de effectiviteit van mediatieve cognitief gedragstherapeutische interventies tegen agitatie bij verpleeghuisbewoners met dementie onderzochten. Twee RCT’s vonden geen effect (Beck, 2002; Visser, 2008) en drie RCT’s vonden een positief effect (Chenoweth, 2014; McCallion, 1999; Sloane, 2004).
|
Zeer laag GRADE |
Er zijn enige aanwijzingen dat een trainingsprogramma gericht op mantelzorgers van mensen met dementie en geagiteerd gedrag die verblijven in de thuissituatie, tot afname van geagiteerd gedrag leidt, drie maanden na de interventie. |
|
Zeer laag GRADE |
Er zijn enige aanwijzingen dat persoonsgerichte omgevingsinterventies (beschikbaarheid van meer op sociale contacten gerichte en vertrouwde ruimtes en op aanpassingen van buitenvoorzieningen) een positief effect hebben op geagiteerd gedrag bij verpleeghuisbewoners met dementie. |
|
Zeer laag GRADE |
Er zijn enige aanwijzingen dat een scholings- en coachingsprogramma gericht op bezoek van verwanten aan verpleeghuisbewoners met dementie, een positief effect heeft op geagiteerd gedrag bij verpleeghuisbewoners met dementie. |
|
Zeer laag GRADE |
Er zijn enige aanwijzingen dat een trainings- en coachingsprogramma voor verzorgenden over ‘persoonsgericht douchen’ en baden met de ‘warme-badhanddoektechniek’ op bed een positief effect hebben op geagiteerd gedrag bij verpleeghuisbewoners met dementie tijdens het wassen. |
Overige interventies
Vier RCT’s onderzochten overige interventies bij verpleeghuisbewoners met dementie en geagiteerd gedrag. Eén RCT vond geen effect (Opie, 2002) en drie RCT’s vonden een positief effect (Cohen-Mansfield, 2012; Garland, 2007; Kovach, 2004) op geagiteerd gedrag bij verpleeghuisbewoners met dementie en geagiteerd gedrag.
|
Zeer laag GRADE |
Er zijn enige aanwijzingen dat het systematisch en op de persoon afgestemd inzetten van (diverse) interventies/activiteiten bij mensen met dementie en geagiteerd gedrag, leidt tot vermindering van geagiteerd gedrag. Hierbij wordt onder andere rekening gehouden met behoeften en mogelijkheden van de patiënt en/of de balans tussen activiteit en rust. |
|
Zeer laag GRADE |
Er zijn enige aanwijzingen dat gesimuleerde aanwezigheid van naasten (via koptelefoon) bij mensen met dementie en geagiteerd gedrag, leidt tot vermindering van geagiteerd gedrag. Dit effect wordt echter ook gevonden bij aanbieding van andere auditieve prikkels (neutraal geluidsfragment en muziek) via een koptelefoon. |
Literatuurconclusies over lichttherapie voor geagiteerd gedrag bij mensen met dementie
|
Laag GRADE |
Er zijn aanwijzingen dat lichttherapie niet effectief is tegen agitatie bij mensen met dementie. |
|
Geen GRADE |
Een verhoogd risico op bijwerkingen bij het toepassen van lichttherapie kan niet worden aangetoond noch uitgesloten. |
Literatuurconclusies psychofarmaca
Klassieke antipsychotica
|
Matig GRADE |
Waarschijnlijk is er een klein positief effect van haloperidol bij de behandeling van agitatie bij mensen met dementie. |
|
Laag GRADE |
Een verhoogd risico op bijwerkingen bij het gebruik van haloperidol bij de behandeling van agitatie bij mensen met dementie (3-16 weken) kan niet worden aangetoond, noch uitgesloten. |
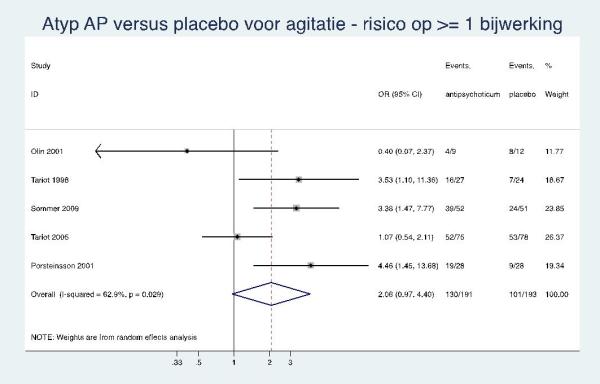
Atypische antipsychotica
|
Laag GRADE |
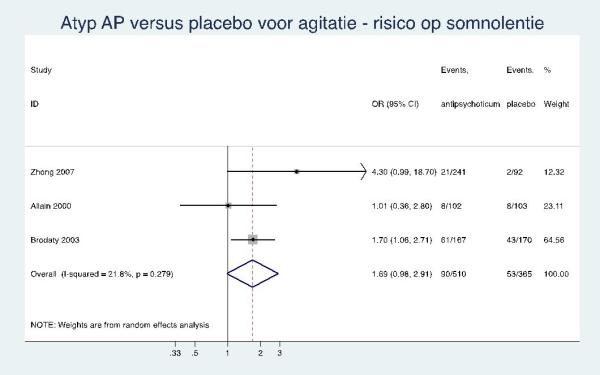
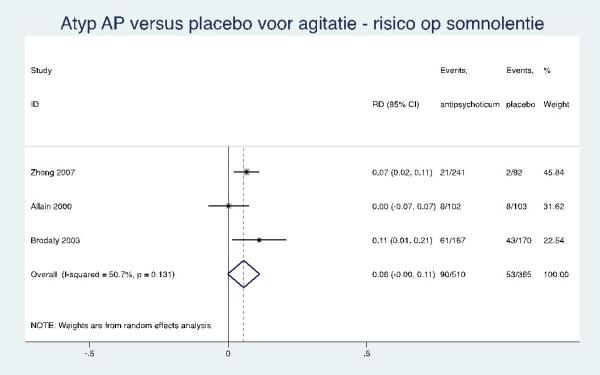
Mogelijk zijn quetiapine en tiapride niet effectief tegen agitatie bij mensen met dementie. Daarentegen zijn er wel aanwijzingen voor een klein positief effect van risperidon bij de behandeling van agressie bij mensen met dementie. |
|
Laag GRADE |
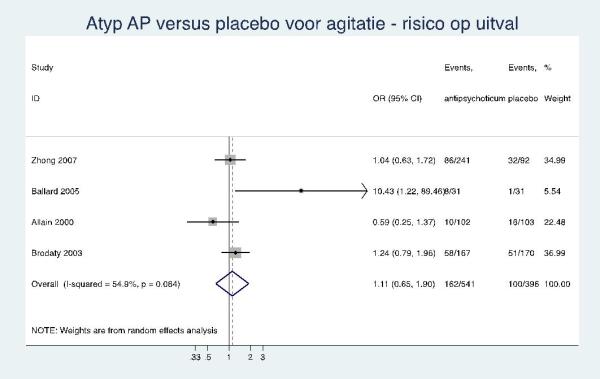
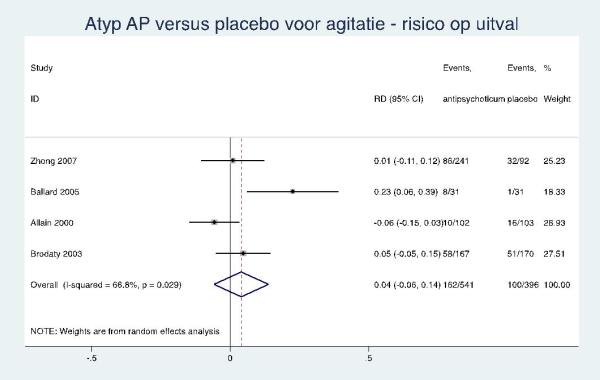
Een verhoogd risico op bijwerkingen bij het gebruik van quetiapine, risperidon en tiapride bij de behandeling van agitatie of agressie bij mensen met dementie (3-10 weken) kan niet worden aangetoond, noch uitgesloten. |
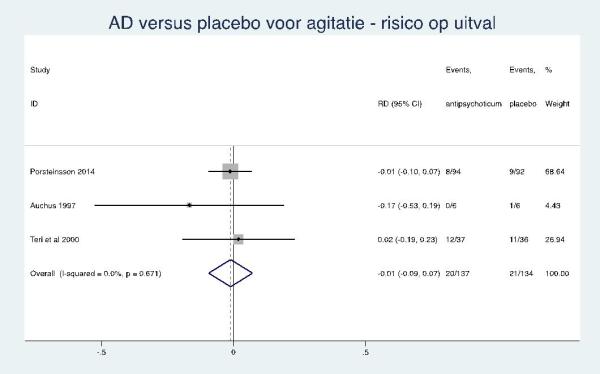
Antidepressiva
|
Laag GRADE |
Er zijn aanwijzingen dat antidepressiva (citalopram en trazodon) niet effectief zijn tegen agitatie bij mensen met de ziekte van Alzheimer. |
|
Laag GRADE |
Er zijn aanwijzingen dat citalopram bij de behandeling van agitatie bij mensen met dementie (6-16 weken) een verhoogd risico op diarree geeft. Een verhoogd risico op overige bijwerkingen kan niet worden aangetoond, noch uitgesloten. |
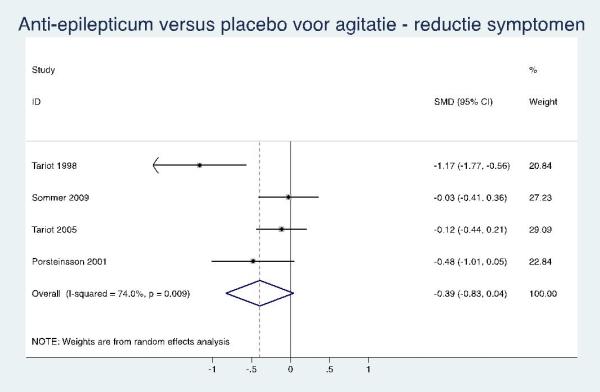
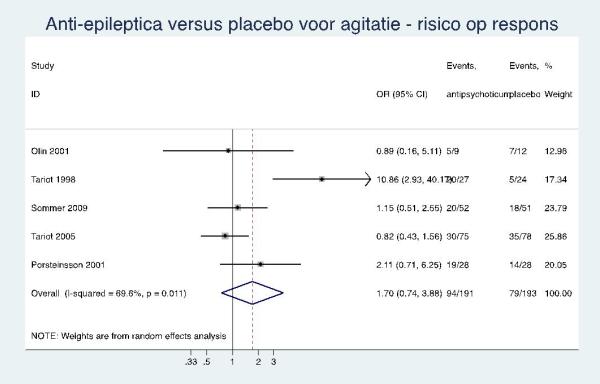
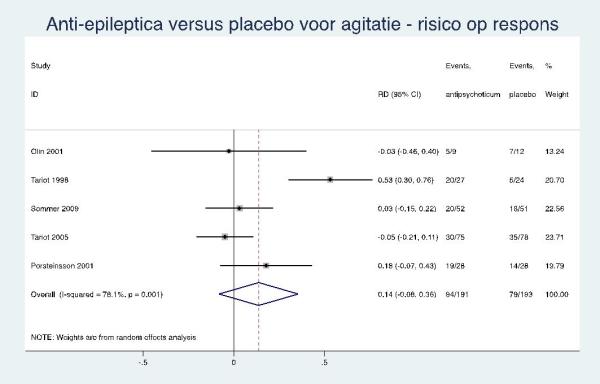
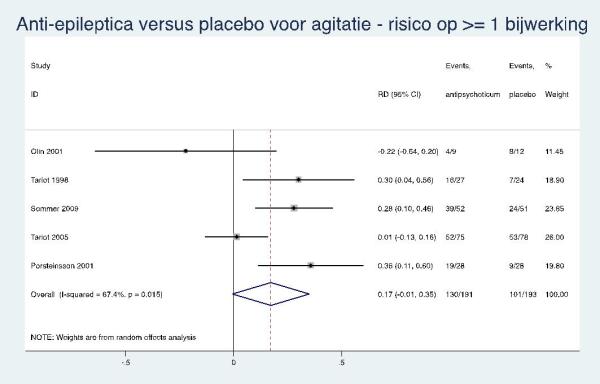
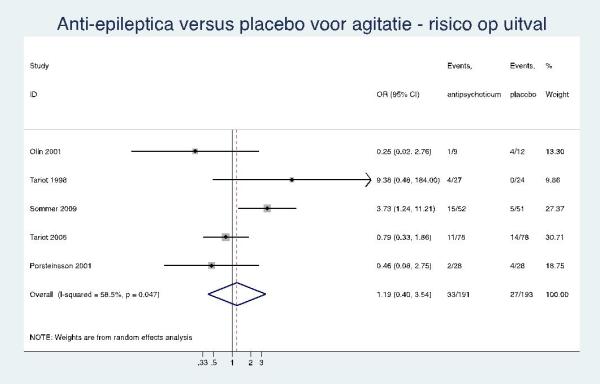
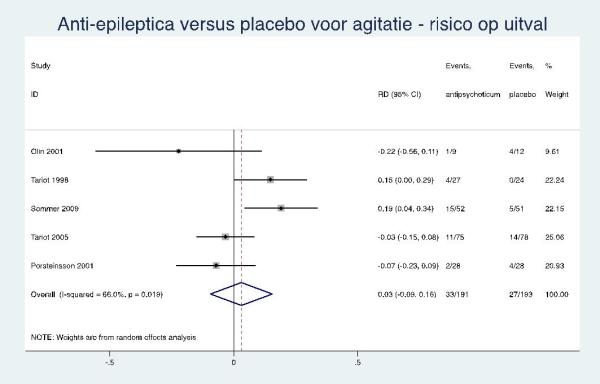
Anti-epileptica
|
Laag GRADE |
Er zijn aanwijzingen dat anti-epileptica niet effectief zijn bij de behandeling van agitatie bij mensen met dementie. |
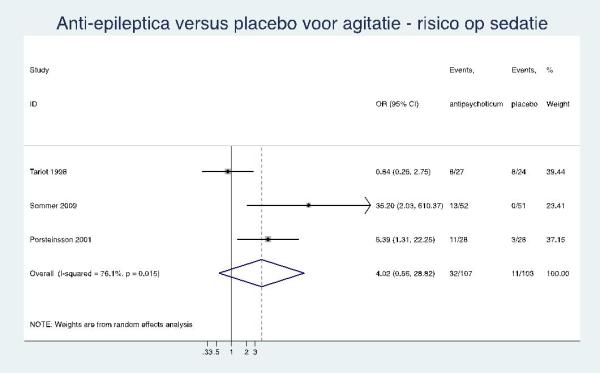
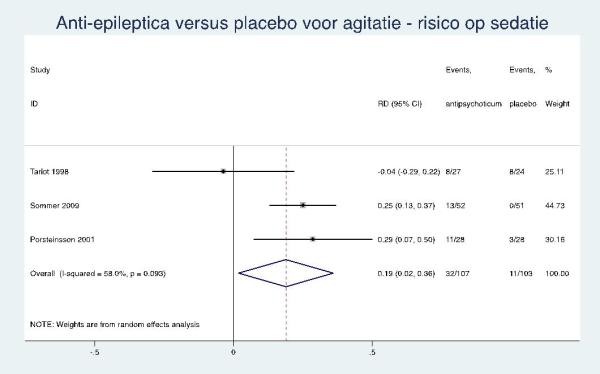
|
Laag GRADE |
Er zijn aanwijzingen voor een verhoogd risico op bijwerkingen en in het bijzonder op sedatie bij het gebruik van anti-epileptica bij de behandeling van agitatie bij mensen met dementie (6-8 weken). |
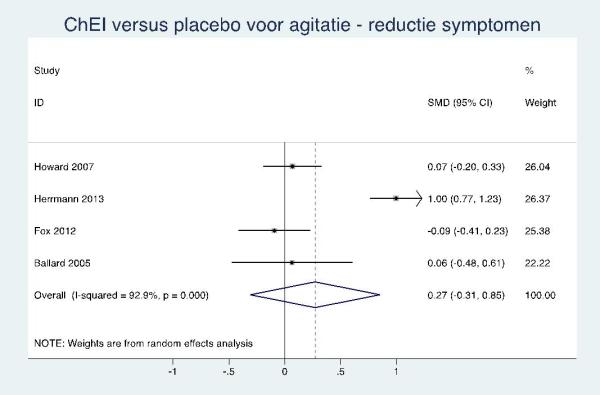
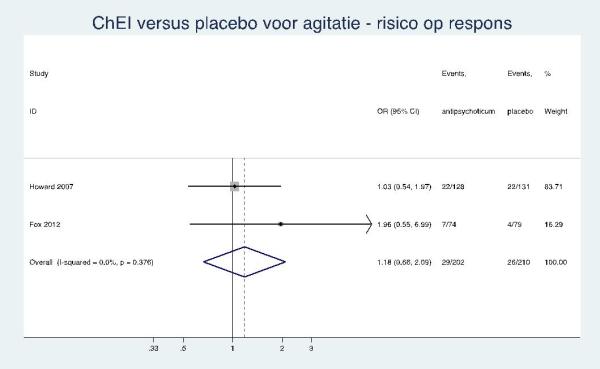
Antidementiemiddelen
|
Laag GRADE |
Er zijn aanwijzingen dat antidementiemiddelen niet effectief zijn tegen agitatie bij mensen met de ziekte van Alzheimer. |
|
Laag GRADE |
Er zijn geen aanwijzingen voor een verhoogd risico op bijwerkingen bij het gebruik van antidementiemiddelen voor de behandeling van agitatie bij mensen met dementie (6-24 weken). |
Zoekvraag (PICO)
Om de eerste uitgangsvraag te kunnen beantwoorden is literatuuronderzoek verricht naar de volgende vraagstelling(en):
“Wat zijn de effecten van psychosociale en psychologische interventies en lichttherapie vergeleken met controle-interventie of gebruikelijke zorg en psychofarmaca vergeleken met placebo op geagiteerd of agressief gedrag bij mensen met dementie?”
De bijbehorende zoekvraag (PICO) is:
- P: mensen met dementie en geagiteerd of agressief gedrag
- I: psychosociale en psychologische interventies, lichttherapie en psychofarmaca
- C: gebruikelijke zorg of controle-interventie voor psychosociale en psychologische interventies en lichttherapie of placebo voor psychofarmaca
- O: reductie van geagiteerd gedrag, percentage patiënten met een klinisch relevant effect (‘responders’), bijwerkingen, uitval
Meer informatie over de opzet van het literatuuronderzoek vindt u onder het tabblad ‘Verantwoording en Methode’. De resultaten voor psychologische, psychosociale interventies en medicamenteuze interventies worden hieronder gepresenteerd en besproken.
Zoeken en selecteren literatuur psychosociale en psychologische interventies
Gevonden RCT’s geagiteerd of agressief gedrag
Op basis van titel en abstract werden 21 reviews geselecteerd voor beoordeling van de gehele tekst. Hiervan beschreven in dertien reviews 29 RCT’s de effecten van psychologische en psychosociale interventies op geagiteerd of agressief gedrag. Uit de buiten de reviews gevonden RCT’s werd van elf nieuwe RCT’s de gehele tekst gelezen. Hiervan werden er vier geïncludeerd (Baillon, 2004; Chenoweth, 2014; Ridder, 2013; Huang, 2013). Zie daarvoor de exclusietabel in bijlage 1.1.
Samenvatting literatuur psychosociale en psychologische interventies deel 1
Kenmerken van geïncludeerde RCT’s
Tabel 1 biedt een overzicht van kenmerken en kwaliteit van de in totaal 33 geïncludeerde RCT's naar de effectiviteit van psychosociale en psychologische interventies voor geagiteerd gedrag bij mensen met dementie. In sommige RCT’s zijn meerdere interventies onderzocht. Hieronder volgt een korte beschrijving.
Activiteitentherapie
Drie RCT’s beschreven effecten van activiteitentherapie (Van der Ploeg, 2013; Lin, 2009; Buettner, 1997) bij in totaal 184 verpleeghuisbewoners.
In een cross-over RCT (n=57) onderzocht Van der Ploeg (2013) de effectiviteit van Montessori-gebaseerde gepersonaliseerde een-op-eenactiviteiten in vergelijking met een controle-interventie van niet-gepersonaliseerde een-op-eenactiviteiten. De vier sessies duurden elk 30 minuten en werden gedurende twee weken twee keer per week gegeven door psychologen en studenten psychologie, waarna gewisseld werd. Gedrag werd geobserveerd (zonder gevalideerde observatie) gedurende 30 minuten voor, tijdens en na afloop van de sessies; aan- of afwezigheid van fysiek niet-agressief gedrag werd met intervallen van één minuut gerapporteerd.
De effectiviteit van een activiteitenprogramma gebaseerd op Montessori is in de driearmige cross-over RCT van Lin (2009) onderzocht bij 91 verpleeghuisbewoners. De activiteiten (n=39) waren gerelateerd aan het dagelijks leven, zoals spellen doen, tafel dekken, was opvouwen en persoonlijke verzorging. Deze vonden volgens protocol plaats, en werden geleid door getraind personeel. Gestart werd met sensorische stimulatie, gevolgd door beweegactiviteiten (die tegelijk met dagelijkse activiteiten werden uitgevoerd) en een afsluiting waarin werd teruggeblikt op de activiteiten. De activiteiten duurden 45 minuten en vonden zes keer per week, gedurende vier weken plaats (bij enkele bewoners waren groepsactiviteiten niet mogelijk en werden individuele activiteiten gedurende vijftien minuten uitgevoerd). Een controlegroep (n=52) ontving zes dagen per week een kwartier aandacht. Naast het activiteitenprogramma werd in een derde groep ook de effectiviteit van acupressuur onderzocht, zie de volgende alinea ‘Sensorische interventies’. Agitatie werd gemeten met de CMAI in de eerste week na de interventie-periode.
In de cross-over RCT (n=36) van Buettner (1996) werden twee vormen van therapeutische recreatie voor verpleeghuisbewoners met elkaar vergeleken: een sensomotorisch programma genaamd ‘Neuro-developmental sequencing program’ (n=18) en een traditioneel activiteitenprogramma (n=18). De activiteiten in het sensomotorisch programma zijn afgestemd op het functieniveau van de bewoner en hebben tot doel hun kracht en flexibiliteit te verbeteren. Beide programma's bestonden uit twaalf groepsactiviteiten per week gedurende vier weken, begeleid door activiteitenbegeleiders en verpleegkundigen. Algehele agitatie is gemeten met de CMAI, afgenomen door verpleegkundige na afloop van het activiteitenprogramma. Agitatie tijdens de activiteiten was geobserveerd door een activiteitenbegeleider met de sectie Behavior van het’ Agitation behavior mapping instrument’.
Muziekinterventies
Negen RCT’s onderzochten de effectiviteit van muziekinterventies bij 480 mensen met dementie en geagiteerd gedrag (Cooke, 2010; Gerdner, 2000; Garland, 2007; Sung, 2006; Groene, 1993; Hicks-Moore, 2008; Remington, 2002; Ridder, 2013; Vink, 2013). Bij drie van de negen RCT’s (Cooke, 2010; Gerdner, 2000; Vink, 2013) bestond de interventie uit alleen muziek. Bij de overige zes RCT’s was er sprake van een combinatie van muziek en andere activiteiten.
De RCT van Cooke (2010) is een cross-over RCT met 47 bewoners met lichte tot matig ernstige dementie. De deelnemers vertoonden in de voorafgaande maand geagiteerd of agressief gedrag, wat bleek uit notities in hun dossier. In de RCT werd een muziekinterventie vergeleken met een controle activiteit. Beide interventies duurden 40 minuten, vonden in groepen plaats, op drie ochtenden per week gedurende acht weken. In de muziekinterventie werd een half uur livemuziek gespeeld door muzikanten, gevolgd door tien minuten afgespeelde muziek. Het muziekrepertoire werd afgestemd op voorkeuren van deelnemers, die werden aangemoedigd actief mee te doen met bijvoorbeeld zingen, hummen, muziekinstrumenten bespelen of bewegen. De controleactiviteit bestond uit leessessies met sociale activiteiten. Een getrainde begeleider was aanwezig en stimuleerde interactie, zoals met korte verhalen lezen/vertellen, moppen vertellen of een korte quiz. De primaire uitkomstmaat was de gemiddelde score op de aangepaste Cohen-Mansfield Agitation Index (CMAI), vier uur na afloop van de sessies.
In de cross-over RCT van Gerdner (2000) werd het effect van een individuele muzieksessie vergeleken met rustige klassieke muziek bij 39 bewoners met (voornamelijk ernstige) dementie. Deelnemers waren verdeeld over een groep (n=16) die eerst zes weken individuele muzieksessies ontving of eerst zes weken naar licht klassieke muziek luisterde, van diverse componisten op advies van een team muziektherapeuten (n=23). De wash-out periode was twee weken. Aan de hand van een vragenlijst, afgenomen bij familieleden, werd de individuele voorkeur voor muziek bepaald. De muziekinterventies duurden een half uur en ze werden twee keer per week aangeboden in een ruimte binnen de instelling waar de cliënt regelmatig verblijft. De interventie vond een half uur voorafgaand aan verwachte piekmomenten van geagiteerd gedrag plaats. Deze verwachte piekmomenten waren vastgesteld op basis van een vijf dagen durende observatieperiode. De agitatie werd gemeten met de aangepaste CMAI, waarbij geagiteerd gedrag elke tien minuten werd gescoord tot een half uur na afloop van de sessies.
In de cross-over RCT van Garland 2007 werd bij verpleeghuisbewoners (n=30) het effect van individuele muziekinterventie vergeleken met gebruikelijke zorg. Er was ook een controle-interventie en er werd een interventie met gesimuleerde aanwezigheid van familie onderzocht (zie ‘overige interventies’). Voor de muziekinterventie werd uitgegaan van muzikale voorkeur uit het verleden. De bewoners kregen een koptelefoon zodat ze vrij konden rondlopen. Ze kregen de interventie een keer per dag, op drie dagen in de week gedurende drie weken. In de interventiegroep werd aanwezigheid van geagiteerd gedrag geobserveerd vijftien minuten voor, tijdens en na afloop van de interventie (45 minuten). In de gebruikelijke zorggroep werd gemeten gedurende 45 minuten waarop geagiteerd gedrag frequent voorkwam (blijkens baseline observaties). Hierbij werd alleen het doelgedrag geobserveerd, dat voor deelnemers kon verschillen. Doelgedrag werd ingedeeld naar fysiek agressief, fysiek niet-agressief, verbaal agressief en verbaal niet-agressief gedrag. Fysiek niet-agressief gedrag kwam het meeste voor.
Vink (2012) onderzocht in een RCT bij 94 deelnemers met lichte cognitieve beperkingen (MCI) tot en met ernstige dementie de effecten van muziektherapie (n=47) in vergelijking met gebruikelijke recreatieve activiteiten (n=47). De groepsinterventie duurde 40 minuten en werd twee keer per week gedurende vier maanden aangeboden in een aparte ruimte (maximaal 34 sessies). De muziektherapie was ten dele geprotocolleerd en startte met een welkomstlied, waarna deelnemers naar muziek luisterden, geselecteerd, gezongen of gespeeld door een getrainde muziektherapeut. Deelnemers werden gestimuleerd mee te zingen, te dansen of een muziekinstrument te bespelen. De muziek was door de therapeut geselecteerd, op basis van tempo en hoeveelheid instrumenten, met als doel plezierige herinneringen op te roepen en agitatie te verminderen. In de controlegroep konden deelnemers recreatieve activiteiten doen, zoals handwerken, sjoelen, koken of puzzelen, met behulp van activiteitenbegeleiders. Agitatie werd vier uur na afloop van de interventies gemeten met de aangepaste CMAI (geagiteerd gedrag op dit moment wel/niet aanwezig in plaats van frequentie van gedrag over de afgelopen twee weken).
In de RCT van Sung (2006) werden 36 bewoners met matige tot ernstige dementie ingedeeld in een groep die muziek met beweging kreeg of een groep die gebruikelijke zorg kreeg, zonder interventie. Deelnemers in de interventiegroep kregen gedurende vier weken, twee keer per week, een half uur een CD te horen met muziek die de meerderheid van de deelnemers waardeerden en die een geschikt ritme en tempo had om bewegingen te stimuleren. Hierbij werden deelnemers gevraagd de bewegingen van de onderzoekers na te doen. De interventie werd in een activiteitenruimte uitgevoerd door een verpleegkundig onderzoeker en getrainde onderzoeksassistenten. Agitatie werd op baseline, en na twee en vier weken, gemeten met een aangepaste CMAI; aanpassing betrof registratie van frequentie van geagiteerd gedrag gedurende een uur direct na de muziekinterventie in plaats van gedurende de voorgaande twee weken.
In de RCT van Groene (1993) namen 32 bewoners met (zeer) ernstige dementie deel met dwaalgedrag. De interventie bestond in de ene groep voornamelijk uit muziekactiviteiten (vijf sessies met muziek, twee met leesactiviteit) en in de andere voornamelijk uit (voor)leesactiviteiten (vijf met voorleesactiviteit, twee met muziek). Voor beide interventies werden de individuele voorkeuren van muziek of lezen van te voren geïnventariseerd en werd de interventie individueel aangeboden in een kleine ruimte op de afdeling, die overigens toegankelijk was voor andere bewoners. Voor elke deelnemer bestond de interventie uit dagelijks één sessie van maximaal vijftien minuten gedurende zeven dagen. De muziekactiviteit kon uit verschillende activiteiten bestaan, waaronder luisteren, zingen en/of dansen, en werd uitgevoerd door de onderzoeker, een ervaren muziektherapeut. In de leessessie werden teksten door de therapeut, en soms door de cliënt, voorgelezen. Dwaalgedrag en zittend gedrag werd geobserveerd door de onderzoeker en op video opgenomen. De uitkomstmaat was hoe lang de cliënt verbleef in de buurt van waar de sessie werd aangeboden (afwezigheid van dwaalgedrag) en dwaalgedrag (afgelegde afstand per uur).
In de RCT van Ridder (2013) werd een cross-over RCT uitgevoerd bij 42 bewoners met matige tot ernstige dementie en geagiteerd gedrag in verpleeghuizen in Denemarken en Noorwegen. Het effect van individuele muziektherapie werd vergeleken met standaardzorg. De individuele muziektherapie werd twee keer per week gegeven (gemiddeld 34 minuten) gedurende zes weken. De meeste sessies vonden in de eigen kamer plaats en werden uitgevoerd door therapeuten met een universitaire opleiding in muziektherapie en ervaring in de dementiezorg. De therapie was gericht op het bevorderen van initiatief nemen, betrokkenheid, zelfexpressie en wederzijds begrip. Naast muziek en zingen, bestond de therapie ook uit andere activiteiten, zoals wandelen of dansen. De agitatie werd gemeten met de CMAI (29 item versie, zowel frequentie als mate van storend gedrag).
In de RCT van Hicks-Moore (2008) werd een RCT uitgevoerd bij 41 bewoners met lichte tot matig ernstige dementie, waarbij een groep drie interventies kreeg: favoriete muziek, handmassage en deze twee interventies gecombineerd. De controlegroep kreeg de gebruikelijke zorg. Elke afzonderlijke interventie duurde tien minuten. Voor de favoriete muziekinterventie werd muziek afgespeeld die in overleg met familie en personeel was gekozen. De handmassage werd vijf minuten op elke hand uitgevoerd volgens een evidence-based protocol (Snyder, 1995). In de gecombineerde interventie werden beide interventies tegelijkertijd uitgevoerd. De interventies werden uitgevoerd door een onderzoeksassistent in de eigen kamer of een vertrouwde ruimte. Agitatie werd gemeten met de aangepaste versie van de CMAI. Observaties vonden plaats tien minuten voorafgaand aan de interventie, tien minuten na afloop van de interventie en een uur post-interventie. In de controlegroep vonden de observaties op dezelfde momenten plaats.
Aan de RCT van Remington (2002) namen 68 bewoners deel met (voornamelijk) matige tot ernstige dementie, met in elk geval twee weken voorafgaand aan de interventie geagiteerd gedrag. Deelnemers werden in een van vier groepen ingedeeld: een die een rustige muziekinterventie kreeg, een die handmassage kreeg, een die beide interventies kreeg en een groep die geen interventie kreeg (de controlegroep). De interventies duurden elk tien minuten en vonden plaats in de eigen kamer of een vertrouwde ontspanningsruimte. Als deelnemers voorafgaand aan de interventie geen geagiteerd gedrag vertoonden, werden ze uitgesloten van deelname. Voor de muziekinterventie werd muziek via een cd-speler afgespeeld. Er werd specifieke muziek uitgezocht om een andere omgeving te creëren en fysiologische reacties op omgevingsstressoren te verminderen (onder meer muziek met rustig tempo, herhaling en zonder impulsgeluiden). De handmassage werd, net als in de RCT van Hicks-Moore, vijf minuten op elke hand gedaan volgens een protocol. Agitatie werd met de aangepast CMAI gemeten, waarbij tien minuten observaties plaatsvonden. Deze vonden plaats voor de interventie, direct na afloop en na een uur.
Zintuiglijke / sensorische interventies
Acht RCT’s onderzochten de effectiviteit van zintuiglijke interventies bij 430 mensen met dementie en geagiteerd gedrag (Baillon, 2004; Hawranik, 2008; Lin, 2009; Moyle, 2014; Hicks-Moore, 2008; Remington, 2002; Fu, 2013; Yang, 2015). Interventies bestonden uit snoezelen, therapeutische aanraking, acupressuur, handmassage en voetmassage.
De cross-over RCT van Baillon (2004) vond plaats bij twintig personen met dementie en geagiteerd gedrag die een dagcentrum bezochten of in een verpleeghuis verbleven. Er werd geloot of deelnemers eerst de zintuiglijke interventie (‘snoezelen’) kregen of reminiscentie. Beide interventies bestonden uit drie sessies in een periode van twee weken. De sessies vonden volgens een protocol plaats, maar waren afgestemd op de individuele deelnemers. De sessies duurden tot 40 minuten, tenzij de patiënt eerder wilde stoppen. De patiënt kreeg telkens dezelfde begeleider, een onderzoeker, die voorafgaand aan de interventies met de patiënt had kennisgemaakt. Tussen beide typen interventies vond een wash-out plaats van één week. Agitatie werd gemeten met het ‘Agitation behaviour mapping instrument’ (Cohen-Mansfield). Hierbij werden observatieperiodes van drie minuten gehanteerd, voorafgaand aan elke sessie en direct na afloop en na 15 en 30 minuten.
In de RCT van Hawranik (2008) werden 51 bewoners verdeeld over drie interventiegroepen: therapeutische aanraking (n=17), gesimuleerde therapeutische aanraking (n=16) en gebruikelijke zorg (n=18). De therapeutische aanraking is gebaseerd op traditionele geneeswijzen, waarbij de therapeut de patiënt aanraakt of de handen enkele centimeters boven de patiënt beweegt (simulatie). De therapeuten waren getraind en voor de gesimuleerde therapeutische aanraking werden vrijwilligers betrokken. Beide interventies werden dagelijks gegeven in sessies van 30 tot 40 minuten gedurende vijf dagen. Elke deelnemer kreeg de interventies van twee verschillende therapeuten. Agitatie werd gemeten met de korte versie van de CMAI, twee uur na de behandeling.
In de RCT van Lin (2009) werd een cross-over trial uitgevoerd bij 133 bewoners met matige tot ernstige dementie naar de effectiviteit van acupressuur in vergelijking met aanwezigheid van een onderzoeker (controlegroep). Er was ook een conditie met Montessori-gebaseerde activiteiten (zie bij activiteiten). Alle behandelingen werden één keer per dag, zes dagen per week gedurende vier weken uitgevoerd. De interventies werden uitgevoerd door getraind personeel, die twaalf weken training hebben ontvangen. De acupressuur werd op vijf acupressuurpunten verricht, na warming-up activiteiten gedurende vijf minuten. In totaal duurde de interventie vijftien minuten. In de controlegroep werd aandacht gegeven gedurende vijftien minuten. Het protocol hiervoor was dat de deelnemer plaatsnam, uitleg kreeg en dat vervolgens diens aandacht in een gesprek werd vastgehouden. Agitatie werd op baseline en posttest gemeten met de CMAI. Hiervoor werden observaties gedurende een week gedaan (van 8-17 uur).
De cross-over RCT van Moyle (2014) werd uitgevoerd bij 55 bewoners met matige tot ernstige dementie. De interventie bestond uit voetmassage die elke doordeweekse dag in de eigen slaapkamer tien minuten volgens een protocol werd uitgevoerd, door een getrainde assistent. Bij de massage werd lichte druk uitgeoefend op tenen, voet en enkel, en er werd een ongeparfumeerde lotion gebruikt. De controle-interventie bestond uit rustige aanwezigheid van een assistent, die geen initiatief nam voor aanraken of een gesprek. De interventies duurden elk drie weken, met een wash-out periode van drie weken.
In de RCT van Hicks-Moore (2008) werd een RCT uitgevoerd bij 41 bewoners met lichte tot matig ernstige dementie met geagiteerd gedrag, waarbij een groep drie interventies kreeg: favoriete muziek, handmassage en deze twee interventies gecombineerd. De controlegroep kreeg de gebruikelijke zorg. Elke afzonderlijke interventie duurde tien minuten. Voor de favoriete muziekinterventie werd muziek afgespeeld, die in overleg met familie en personeel was gekozen. De handmassage werd vijf minuten op elke hand uitgevoerd volgens een evidence-based protocol (Snyder, 1995). In de gecombineerde interventie werden beide interventies tegelijkertijd uitgevoerd. De interventies werden uitgevoerd door een onderzoeksassistent en vonden plaats in de eigen kamer of een vertrouwde ruimte in de instelling. Agitatie werd gemeten met de aangepaste versie van de CMAI. Observaties vonden plaats tien minuten voorafgaand aan de interventie, tien minuten na afloop van de interventie en een uur post-interventie. In de controlegroep vonden de observaties op dezelfde momenten plaats.
De RCT van Remington (2002) werd uitgevoerd bij 68 bewoners met (voornamelijk) matige tot ernstige dementie, die twee weken voorafgaand aan de interventie geagiteerd gedrag hadden vertoond. Deelnemers werden in een van vier groepen ingedeeld: een die een rustige muziekinterventie kreeg, een die handmassage kreeg, een die beide interventies kreeg en een groep die geen interventie kreeg (de controlegroep). De interventies duurden elk tien minuten en vonden plaats in de eigen kamer of een vertrouwde ontspanningsruimte. Als deelnemers voorafgaand aan de interventie geen geagiteerd gedrag vertoonden, werden ze uitgesloten van deelname. Voor de muziekinterventie werd muziek via een cd-speler afgespeeld. Er werd specifieke muziek uitgezocht om een andere omgeving te creëren en fysiologische reacties op omgevingsstressoren te verminderen (onder meer muziek met rustig tempo, herhaling en zonder impulsgeluiden). De handmassage werd, net als in de RCT van Hicks-Moore, vijf minuten op elke hand gedaan volgens een protocol. Agitatie werd met de aangepast CMAI gemeten, waarbij tien minuten observaties plaatsvonden. Deze vonden plaats voor de interventie, direct na afloop en na een uur.
In de driearmige RCT met parallelle groep design van Fu (2013; n=44) werd handmassage met aromatherapie vergeleken met waterspray (controlegroep). De handmassage vond geprotocolleerd plaats (Snyder, 1995) en duurde tweeënhalve minuut per hand. De controlegroep kreeg een waterspray. Interventies vonden dagelijks twee keer plaats (ochtend en middag) gedurende zes weken. De therapie werd in een rustige, afgezonderde ruimte, bijvoorbeeld de eigen kamer, gegeven door de onderzoeker en zes getrainde onderzoeksassistenten. (Niet)Agressief en geagiteerd gedrag werden gemeten met de verkorte CMAI.
Effectiviteit van acupressuur met aromatherapie is onderzocht in de parallelle groep trial van Yang (2015; n=113). Bij bewoners in de interventiegroep (n=56) werd vier weken lang, eenmaal per dag, lavendelolie (2,5%) aangebracht op vijf acupunten. Op deze punten werd gedurende twee minuten druk uitgeoefend (acupressuur). De controlegroep (n=57) ontving gebruikelijke zorg. Agitatie werd gemeten met de CMAI-vragenlijst.
Aromatherapie
Zes RCT’s over aromatherapie werden geïncludeerd (Lin, 2007; O’Connor, 2013; Yang, 2015; Burns, 2011; Ballard, 2002; Fu, 2013). Alle zes RCT’s vonden plaats binnen instellingen, bij in totaal 538 bewoners.
De effectiviteit van aromatherapie middels diffusers, gevuld met 100% lavendelolie, is met een cross-over design onderzocht door Lin (2007; n=70). De aromadiffusers met lavendelolie of placebo (zonnebloemolie) werden 's nachts aan beide zijden van het hoofdkussen van de bewoners geplaatst gedurende drie weken. Agitatie werd gemeten met de CMAI-vragenlijst.
In de cross-over trial van O’Connor (2013; n=66) werden gedurende één week driemaal beide onderarmen van de bewoners gemasseerd met een lavendelolie (30%) of placebo (jojobaolie). Agitatie werd gemeten met de ‘Philadelphia geriatric center affect rating scale’ (PGCARS) en met gedragsobservaties.
De effectiviteit van aromatherapie met lavendelolie is onderzocht in de parallelle groep trial van Yang (2015; n=130). Bij bewoners in de interventiegroep (n=73) werd vier weken lang eenmaal per dag lavendelolie (2,5%) aangebracht op vijf acupunten. De controlegroep (n=57) ontving gebruikelijke zorg. Agitatie werd gemeten met de CMAI-vragenlijst.
Burns (2011; n=77) onderzocht in een RCT met parallelle groep design de effectiviteit van een lotion met 10% citroenmelisse. De handen en bovenarmen van bewoners werden gedurende twaalf weken ingesmeerd met een lotion met citroenmelisse of placebo (zonnebloemolie). Agitatie werd gemeten met de ‘Pittsburgh agitation scale’ (PAS).
In de RCT met parallelle groep design van Ballard (2002; n=72) werd de effectiviteit van een lotion met 10% citroenmelisse vergeleken met een placebointerventie (zonnebloemolie). Gedurende vier weken werden gezicht en armen van bewoners ingesmeerd. Agitatie werd gemeten met de CMAI-vragenlijst, de subschaal ‘Agitatie’ van de ‘Neuropsychiatrische vragenlijst’ (NPI) en ‘Dementia care mapping -observaties’ (DCM).
In de driearmige RCT met parallelle groep design van Fu (2013; n=45) werd aromatherapie (n=23) vergeleken met een waterspray (controlegroep; n=22). De aromatherapie werd volgens richtlijnen gegeven om huidirritatie te voorkomen (3% essentiële lavendelolie, drie keer per interventie gesprayd op de borst, van 30 cm afstand). De controlegroep kreeg de spray op dezelfde wijze. De interventies vonden dagelijks twee keer plaats (ochtend en middag), gedurende zes weken. De therapie werd in een rustige, afgezonderde ruimte, bijvoorbeeld de eigen kamer, gegeven door de onderzoeker en zes getrainde onderzoeksassistenten. (Niet)Agressief en geagiteerd gedrag werden gemeten met de verkorte CMAI.
Mediatieve cognitief gedragstherapeutische interventies
In negen RCT’s is effectiviteit van mediatieve gedragstherapeutische interventies onderzocht bij 1338 mensen met dementie en geagiteerd gedrag. Vier RCT’s vonden plaats in de thuissituatie (Gormley, 2001; Huang, 2013; Huang, 2003; Wright, 2001), de overige vijf RCT’s waren gericht op patiënten verblijvend in een instelling (Chenoweth, 2014; McCallion, 1999; Sloane, 2004; Visser, 2008; Beck 2002).
De mediatieve gedragstherapeutische interventies voor thuiswonende patiënten (n=343) waren er allemaal op gericht de mantelzorger te leren omgaan met geagiteerd gedrag van hun naaste.
Een gedragsmanagementprogramma voor mantelzorgers tegen agressief gedrag van hun naaste met dementie werd onderzocht door Gormley (2001; n=62). Het programma werd uitgevoerd door een van de auteurs en bestond uit vier sessies over een periode van acht weken. In de eerste sessie leerden mantelzorgers de gedragsproblemen te zien in de context van de geheugenaandoening en zij leerden de uitlokkende dan wel in stand houdende factoren te achterhalen. Op basis van deze analyse werd in de volgende sessies een individueel afgestemde gedragsinterventie ontwikkeld, bestaande uit: 1) vermijden of veranderen van de uitlokkende of in stand houdende factoren, 2) gebruik van juiste communicatietechnieken, 3) bevestigen of aanvaarding van onjuiste verklaringen of ongepaste verzoeken, en/of 4) gebruik van afleidingstechnieken. De controlegroep ontving van dezelfde auteur een gelijk aantal sessies gevuld met discussies over zorggerelateerde onderwerpen en advies over beschikbaarheid van lokale wettelijke en vrijwillige diensten. Agressie werd gemeten twee weken na afloop van het programma met de ‘Rating scale for agressive behaviour in the elderly’ (RAGE).
Huang (2003; n=59) onderzocht de effectiviteit van een trainingsprogramma voor mantelzorgers voor verbeteren van de zelfeffectiviteit en het verminderen van gedragsproblemen gebaseerd op het ‘Progressively lowered stress threshold model’ (PLST). Dit richt zich op het aanpassen van eisen van de omgeving om stress te verminderen en het bevorderen van aangepast gedrag van de mensen met dementie. Het trainingsprogramma (n=30) was gericht op het helpen van mantelzorgers in het identificeren van de tijd en frequentie van specifieke gedragsproblemen van hun naaste, het nagaan van oorzakelijke stressoren en het aanpassen van de omgeving en het dagelijks schema. De training werd gegeven door een geriatrieverpleegkundige (tevens onderzoeker) en vond plaats in twee sessies van twee tot drie uur, bij de mantelzorger thuis. De twee trainingssessies vonden een week na elkaar plaats. Na afloop van de training ontvingen zij wekelijkse telefonische consultaties gedurende drie maanden. Mantelzorgers in de controlegroep (n=29) ontvingen alleen sociale telefoongesprekken en algemene informatiefolders over dementie. Agitatie werd gemeten drie weken en drie maanden na afloop van de training.
Huang (2013; n=129) onderzocht een geïndividualiseerd trainingsprogramma aan huis voor mantelzorgers van mensen met dementie en probleemgedrag (CMAI≥50). Het programma was gericht op het vergroten van de bekwaamheid van de mantelzorgers (n=63) in het omgaan met gedragsproblemen en het verminderen van probleemgedrag van de naaste met dementie. De training werd in twee sessies gegeven door een speciaal geschoolde sociaal- of geriatrieverpleegkundige, bij de mantelzorger thuis. Beide sessies vonden een week na elkaar plaats. Weer een week later en daarna maandelijks ontvingen zij telefonische consulten. Ook ontvingen de mantelzorgers een zorggids met informatie over veelvoorkomende gedragsproblemen en hoe hiermee om te gaan. Mantelzorgers in de controlegroep (n=66) kregen één huisbezoek, ontvingen een algemene informatiegids over dementie zonder specifieke informatie over probleemgedrag en sociale telefoontjes. Fysiek agressief gedrag is gemeten met de gelijknamige subschaal van de CMAI. Deze subschaal is gedichotomiseerd in ‘fysiek agressief gedrag’ (score≥8) en ‘geen fysiek agressief gedrag’ (score=7). De metingen zijn afgenomen twee weken na de laatste trainingssessie en na drie en zes maanden follow-up.
Wright (2001; n=93) onderzocht de effectiviteit van een éénjarig verpleegkundig opleidings- en begeleidingsprogramma voor mantelzorgers (n=68) van ouderen die, na opvang in een ‘Behavioral intensive care unit’ (BICU) vanwege storend gedrag, weer naar huis gingen. De mantelzorgers in de controlegroep (n=25) kregen geen interventie aangeboden. Het programma werd uitgevoerd door een geriatrisch of psychiatrisch verpleegkundige specialist. De verpleegkundige vroeg de mantelzorger aan te geven wat de meest problematische gedragingen zijn. Daarna werden strategieën besproken hoe hiermee om te gaan en werd een plan gemaakt voor de mantelzorger om de nieuwe aanpak uit te voeren. Daarnaast richt de interventie zich ook op de emotionele en fysieke gezondheid van de mantelzorger met behulp van ondersteunende begeleiding. Agitatie werd gemeten door dezelfde verpleegkundige met behulp van de CMAI, na één, twee, drie, zes en twaalf maanden.
De mediatieve interventies tegen agitatie in de vijf RCT’s (n=995) bij verpleeghuisbewoners waren zeer divers.
McCallion (1999; n=66) onderzocht de effectiviteit van het ‘Family visit education program’ voor familieleden van verpleeghuisbewoners met dementie en geagiteerd gedrag, zoals fysieke agressie, schelden, storende geluiden of motorische rusteloosheid. Het programma (n=32) was gericht op verbale communicatie, non-verbale communicatie en effectief structureren van de familiebezoeken. Het bestond uit vier groepssessies van anderhalf uur en drie familiebijeenkomsten van één uur en duurde in totaal acht weken. Het programma is vergeleken met gebruikelijke zorg in een wachtlijstcontrolegroep (n=34). De CMAI is door twee personen (niet-deelnemende observator en verpleegkundige) afgenomen na drie en zes maanden.
Effectiviteit van persoonsgerichte zorg en een persoonsgerichte omgeving op agitatie bij bewoners met dementie is door Chenoweth (2014; n=601) onderzocht in een vierarmige trial. Na screening van 89 instellingen met de ‘Person-centred environment and care assessment tool’ (PCECAT) zijn de 38 instellingen met de meeste ruimte voor verbetering geïncludeerd in de RCT. Deze instellingen zijn gerandomiseerd naar persoonsgerichte zorg (n=155), op persoon afgestemde omgeving (n=154), persoonsgerichte zorg en omgeving (n=150) of gebruikelijk zorg en omgeving (n=142). Voor de persoonsgerichte zorg kregen vijf stafleden 32 uur externe training. Deze training was gericht op aandacht voor de gevoelens van de bewoner bij agitatie, persoonsgerichte interactie met de bewoner en gebruik van persoonsgerichte zorgplanning om zo in de psychosociale behoeften van de bewoner te voorzien. Voor de persoonsgerichte omgeving waren er twee experts die zorgden voor de planning, implementatie en evaluatie met behulp van de ‘Environmental audit tool’. Denk daarbij aan verbeteringen in de veiligheid, toegankelijkheid en gebruik van buitenruimtes, aanbod van een grotere variëteit aan sociale ruimtes, gebruik van kleuren en voorwerpen voor wegwijzing en vergroten van gevoel van vertrouwdheid. Instellingen in de controlegroep werden alleen gemonitord. De instellingen kregen vier maanden de tijd voor de interventie en om alle plannen te implementeren. Agitatie is gemeten direct na afloop van interventie en na acht maanden met CMAI.
De RCT van Sloane (2004) onderzocht agitatie tijdens het wassen. In deze RCT zijn patiëntgericht douchen en een ‘handdoekbad’ vergeleken met gebruikelijke zorg met behulp van washandjes bij 73 verpleeghuisbewoners. Het ‘handdoekbad’ is een verzorgingswijze op bed met behulp van warme, natte en zachte badhanddoeken, die op de persoon worden gelegd en waarmee deze zacht wordt gemasseerd. Het patiëntgericht verzorgen beoogt de ervaring van de patiënt te individualiseren met onder andere het voorleggen van keuzes, bedekken met een handdoek tegen warmteverlies, aandacht afleiden, gebruik van badproducten op advies van familie, gebruik van zeep die niet afgespoeld hoeft te worden en aanpassen van de waterstraal. Bij de op bed uitgevoerde handdoekbad-methode maakt de zorgverlener gebruik van twee badlakens, twee badhanddoeken, niet-afspoelende zeep en twee liter water. De zorgverlener houdt de patiënt bedekt en wast het lichaam middels een zachte massage. Douchen zonder patiëntgerichte training fungeerde als controleconditie. De interventieperiode van zes weken bestond uit een trainings- en coachingsperiode van vier weken, gevolgd door een periode van twee weken waarin het baden werden gefilmd. Agitatie en agressie tijdens het wassen werd beoordeeld met het ‘Care recipient behavior assessment-systeem’ (CAREBA), voor beoordeling van gedragssymptomen gebaseerd op de CMAI.
Visser (2008) onderzocht de effectiviteit van personeelstraining met en zonder intercollegiaal peer support. Het opleidingsprogramma voor verpleeghuismedewerkers stimuleert een gepersonaliseerde aanpak bij het omgaan met gedrag en bestond uit acht wekelijkse bijeenkomsten van één à anderhalf uur. De eerste drie bijeenkomsten waren didactisch van aard, gevolgd door vijf workshops waarin geïndividualiseerde zorgplannen werden ontwikkeld. Bij een deel van de interventiegroep kreeg het personeel peer support aangeboden. Het peersupportprogramma was gericht op de werkstress en andere problemen die verzorgenden ervaren in de zorgverlening en bestond uit vier sessies van een half uur, aansluitend aan de laatste vier educatiebijeenkomsten. Er namen 52 professionals (educatie 10; educatie + peer support=17; controle=25) en 76 patiënten (educatie 21; educatie + peer support=23; controle=32) deel aan de trial. CMAI is ingevuld direct na de interventie. Na drie en zes maanden volgde de follow-up.
In de RCT van Beck (2002; n=179) werden verschillende gedragsinterventies onderzocht die gericht waren op uitlokkers van gedragsontregelingen en op psychosociale behoeften van mensen met matige tot ernstige dementie. Zij werden verdeeld over vijf groepen: drie interventiegroepen, een controlegroep bestaande uit 30 minuten interactie met een verzorger en een gebruikelijke zorggroep. De drie interventies bestaan uit: 1) dagelijks 45-60 minuten een geprotocolleerde interventie door verzorgenden waarin gedrag- en communicatiestrategieën werden toegepast om probleemgedrag tijdens de ADL te verminderen; 2) een psychosociale interventie van 30 minuten waarbij verzorgers 25 standaardmodules systematisch leerden toepassen. Elke module richt zich op vijf psychosociale gebieden (bijvoorbeeld uiten van gevoelens, ontspanning) en kent vijf zintuiglijke modaliteiten (bijvoorbeeld verbaal, visueel); 3) een combinatie van deze twee therapieën. Alle interventies werden uitgevoerd door verpleeghulpen, onder supervisie van een gerontologische verpleegkundig specialist. De interventies vonden vijf dagen per week plaats gedurende zeven weken, exclusief een gewenningsperiode en periode van afronden van de interventie. Vermindering van storend gedrag werd direct na de interventie gemeten en één en twee maanden later met de ‘Disruptive behaviour scale’ (Beck, 1997).
Samenvatting literatuur psychosociale en psychologische interventies deel 2
Overige interventies
In vier RCT’s werden overige interventies onderzocht bij in totaal 360 mensen met agitatie en dementie: Garland, 2007, Opie, 2002, Kovach, 2004 en Cohen-Mansfield, 2012. Deze interventies bestonden uit: 1) gesimuleerde aanwezigheid van familie, 2) op de persoon afgestemde (combinatie van) interventies op het gebied van medicatie, verzorging/benaderingswijze en psychosociaal, 3) het in balans houden van arousal door gericht activiteiten aan te bieden, en 4) een systematische methode voor het op maat aanbieden van niet-farmacologische behandelingen.
In een cross-over RCT van Garland 2007 werd bij verpleeghuisbewoners (n=30) het effect van gesimuleerde aanwezigheid van familie vergeleken met een controle-interventie en gebruikelijke zorg (er werd ook een muziekinterventie onderzocht, zie aldaar).
De gesimuleerde aanwezigheidsinterventie bestond uit vijftien minuten luisteren naar geluidsfragmenten waarin een familielid vertelt over positieve ervaringen uit het verleden. Het fragment was samengesteld op basis van een interview door een getrainde psycholoog over het leven van de bewoner. De controle-interventie bestond uit vijftien minuten luisteren naar een geluidsfragment waarin een onbekende op neutrale wijze een tekst over tuinieren voorleest. De bewoners kregen een koptelefoon zodat ze vrij konden rondlopen. Ze kregen de interventie een keer per dag, op drie dagen in de week, gedurende drie weken. Aanwezigheid van geagiteerd gedrag werd geobserveerd vijftien minuten voor, tijdens en na afloop van de interventies (45 minuten) en in de gebruikelijke zorggroep gedurende 45 minuten waarop geagiteerd gedrag frequent voorkwam (blijkens baseline observaties). Hierbij werd alleen het doelgedrag geobserveerd, dat voor deelnemers kon verschillen. Doelgedrag werd ingedeeld naar fysiek agressieve agitatie, fysiek niet-agressieve agitatie, verbaal agressieve agitatie en verbaal niet-agressieve agitatie. Fysiek niet-agressief gedrag kwam het meeste voor.
Opie (2002) onderzocht de meerwaarde van op de persoon afgestemde multidisciplinaire interventies bij verpleeghuisbewoners die meerdere keren per dag matig ernstig probleemgedrag vertoonden. De interventie werd uitgevoerd door een team van vier leden met een psychiatrische, psychologische of verpleegkundige achtergrond. Er vond een uitgebreide inventarisatie van relevante gegevens plaats en het team voerde een half uur overleg. Dit resulteerde in een plan om met het probleemgedrag om te gaan. Drie typen behandelingen werden aangeboden, alleen maar meestal in combinatie: medicatie (bijvoorbeeld psychofarmaca of pijnmanagement), verzorging/benaderingswijze (bijvoorbeeld voeding, communicatie) of psychosociaal (bijvoorbeeld gedragsbeïnvloeding, reminiscentie, aromatherapie). Er werd geloot wie deze assessment en interventies vroegtijdig kreeg en wie dit later kreeg aangeboden (wachtlijstcontrole). Geagiteerd gedrag werd geobserveerd met de CMAI (gedurende vijftien minuten, drie keer per dag) en met de ‘Behaviour assessment graphical system (BAGS)’. Daarbij wordt elk uur de frequentie en ernst van gedragsproblemen geïnventariseerd, gedurende 24 uur. Beide observaties werden drie dagen per week gedurende vier weken gedaan.
Kovach (2004; n=102) onderzocht de effectiviteit van de ‘Balancing arousal controls excesses-interventie’ (BACE), ofwel activiteiten gericht op het verminderen van overmatige of ondermaatse spanning. Bij bewoners in de BACE-interventiegroep (n=36) werd het dagelijks activiteitenschema van een persoon aangepast om zo te komen tot een meer optimale 'arousal'. Hierbij werd binnen één week de arousal-balans beoordeeld door een geriatrieverpleegkundige in samenwerking met een eerstverantwoordelijk verpleegkundige (EVV). Bij onbalans werd vervolgens een plan gemaakt en een nieuw activiteitenschema opgesteld en geïmplementeerd. Bij personen in de controlegroep (n=24) werd het activiteitenschema niet aangepast. Van de 24 uitvallers is niet gerapporteerd in welke groep zij zaten. Agitatie werd gemeten aan het eind van de interventieweek door middel van observaties gerapporteerd op een VAS-schaal.
Cohen-Mansfield (2012) onderzocht een systematische methode om niet-farmacologische behandelingen op maat aan te bieden: ‘Treatment route for exploring agitation’ (TREA). Op basis van diverse informatiebronnen werd een hypothese geformuleerd over onvervulde behoeften, waarop een interventie op maat werd voorgesteld. Daarbij werd rekening gehouden met interesses, voorkeuren en vroegere identiteit (TREA-beslisboomprotocol). Een getrainde onderzoeksassistent voerde observaties uit en gaf adviezen over interventies aan het personeel. Er werden verschillende interventies getest en degene die het meest relevant leek, werd vervolgens toegepast gedurende de twee weken interventieperiode en tijdens de vier uur op de dag waarop geagiteerd gedrag het meest voorkwam (deze uren waren vastgesteld op basis van observaties tijdens de baselineperiode). Diverse interventies konden worden ingezet, zoals groepsactiviteiten, gesimuleerde aanwezigheid, spellen, beweging, consult van arts en voeding. Het personeel in de controlegroep kreeg een algemene training over (de herkomst van) geagiteerd gedrag van bewoners en over niet-farmacologische interventies. Er deden 125 mensen met dementie met agitatie of agressie mee uit negen verpleeghuizen. Zij kregen een interventie op maat (n=89) of een controle-interventie (n=36). De agitatie of agressie werd gemeten met de ‘Agitation behavior mapping instrument’ (ABMI) gedurende de eerste drie en laatste drie dagen van de interventieperiode.
Tabel 1. Kenmerken en kwaliteit van RCT’s naar effectiviteit van psychosociale en psychologische interventies voor geagiteerd gedrag bij mensen met dementie
|
Publicatie |
Therapie |
Setting |
Dementie (ernst; type) |
Agitatie (ernst; criteria) |
N (I/C) |
Behandelduur |
Meetinstrument; follow-up direct na afloop van interventie tenzij anders vermeld |
Kwaliteit opzet & uitvoering1 |
|
Activiteitentherapie |
||||||||
|
Van der Ploeg, 2013 |
Gepersonaliseerde een-op-een activiteiten |
Instelling |
Diagnose dementie |
Fysieke agitatie op verschillende momenten buiten de verpleegmomenten |
57 (21/36) |
4 wkn. |
Observaties van fysiek niet-agressief gedrag (per min. gedurende half uur); |
3/6 |
|
Lin, 2009 |
Montessori-gebaseerde activiteiten |
Instelling |
Diagnose dementie |
CMAI≥35 |
91 (39/52) |
4 wkn. |
CMAI |
4/6 |
|
Buettner, 1996 |
Sensomotorisch activiteitenprogramma |
instelling |
Ernstige dementie |
Onduidelijk |
36 (18/18)
|
4 wkn. |
CMAI; observaties m.b.v. Agitation Behavior Mapping Instrument – sectie Behavior |
2/6 |
|
Muziekinterventies |
||||||||
|
Cooke, 2010 |
Muziekinterventie (groep) |
Instelling |
lichte tot matig ernstige dementie (MMSE 12 -24) |
Notitie in dossier van geagiteerd/ agressief gedrag afgelopen maand |
47 (24/23) |
8 wkn. |
CMAI-SF; direct na afloop interventie |
3/6 |
|
Gerdner, 2000 |
Muziekinterventie (individueel en groep) |
Instelling |
Lichte tot ernstige dementie (GDS 3-7) |
Aanwezigheid van geagiteerd gedrag (o.a. Temporal Patterning Assessment of Agitation (TPAA) |
39 (16/23) |
6 wkn. |
CMAI aangepaste versie; half uur tijdens en half uur post interventie |
1/6 |
|
Garland, 2007 |
Muziektherapie (individueel) |
Instelling |
Dementie |
Meerdere keren per dag geagiteerd gedrag in voorgaande 2 wkn. (CMAI door personeel) |
30 |
4 wkn. |
Frequenties van fysieke en verbale (niet)agressieve agitatie; 15 min tijdens interventie (data 15 min post interventie niet bruikbaar) |
2/6 |
|
Vink, 2012 |
Muziektherapie (groep) |
Instelling |
MCI tot ernstige dementie (GDS 3-7) |
Hoge mate geagiteerd gedrag (CMAI>44) |
94 (47/47) |
4 mnd. |
CMAI aangepaste versie; 4 uur post interventie |
2/6 |
|
Sung, 2006 |
Muziek en bewegen |
Instelling |
MCI tot matig ernstige dementie (GDS 3-6) |
Aanwezigheid van geagiteerd gedrag volgens CMAI |
40 |
4 wkn. |
CMAI-aangepaste versie; week 2 en 4 |
3/6 |
|
Groene, 1993 |
Muziek |
Instelling |
Matig-ernstige tot Ernstige dementie (GDS 6-7) |
Aanwezigheid dwaalgedrag volgens personeel |
32 |
15 wkn. (interventieduur 1 week) |
Verblijf in buurt van sessie; loopgedrag (afstand/uur) tijdens sessie |
1/6 |
|
Ridder, 2013 |
Muziek |
Instelling |
Matig ernstige tot ernstige dementie |
Aanwezigheid van symptomen van agitatie |
42 |
6 wkn. |
CMAI; in week na interventie
|
3/6 |
|
Hicks-Moore, 2008 |
Muziek |
Instelling |
Lichte tot matig ernstige dementie |
Aanwezigheid van geagiteerd gedrag volgens (aangepaste) CMAI |
41 |
3 x 10 min. |
CMAI aangepaste versie; post interventie en een uur later |
1/6 |
|
Remington 2002 |
Muziek |
Instelling |
Lichte tot ernstige dementie |
Aanwezigheid van geagiteerd gedrag volgens (aangepaste) CMAI |
34 |
10 min. |
CMAI aangepaste versie; post interventie en een uur later |
3/6 |
|
Zintuiglijke interventies |
||||||||
|
Baillon, 2004 |
Snoezelen |
Instelling of dagcentrum |
Ernstige dementie |
Bekend met gedragsproblemen (geagiteerd gedrag volgens CMAI) |
25 |
5 wkn. |
ABMI (Agitation Behaviour Mapping Instrument); postinterventie en 15 en 30 min later |
0/6 |
|
Hawranik, 2008 |
Therapeutische aanraking |
Instelling |
Mensen met Alzheimer dementie |
Geagiteerd gedrag volgens verzorgende (gedurende afgelopen maand of langer bekend met geagiteerd gedrag) |
94 (42/52) |
5 dgn. |
CMAI korte versie 2 uur na elke behandeling |
2/6 |
|
Lin, 2009 |
Acupressuur |
Instelling |
Matige tot ernstige dementie |
Aanwezigheid van geagiteerd gedrag volgens CMAI (score > 35) |
133 |
6 wkn. |
CMAI; posttest |
3/6 |
|
Moyle, 2014 |
Voetmassage |
Instelling |
Matige tot ernstige dementie |
Bekend met geagiteerd gedrag volgens Pittsburgh Agitation Scale |
55 |
3 wkn. |
CMAI; posttest |
3/6 |
|
Hicks-Moore, 2008 |
Handmassage (individueel) |
Instelling |
Lichte tot matig ernstige dementie |
Aanwezigheid van geagiteerd gedrag volgens (aangepaste) CMAI |
41 |
3 x 10 min. |
CMAI aangepaste versie; post interventie en een uur later |
1/6 |
|
Remington, 2002 |
Massage (individueel) |
Instelling |
Lichte tot ernstige dementie |
Aanwezigheid van geagiteerd gedrag volgens (aangepaste) CMAI |
34 |
10 min. |
CMAI aangepaste versie; post interventie en een uur later |
3/6 |
|
Fu, 2013 |
Handmassage met lavendelolie
|
instelling |
MMSE≤24 (ernstig 29%, matig ernstig37,7%, licht 14,7%); AD |
gedocumenteerde voorgeschiedenis, min. 14 dgn. (los of aaneengesloten) agitatie/agressie in afgelopen 3 mnd. |
44 (22/22)
|
6 wkn. |
CMAI-SF (short form); direct na afloop van interventie |
2/6 |
|
Yang, 2015 |
Acupressuur met lavendelolie |
Instelling |
diagnose dementie door neuroloog of psychiater volgens DSM-IV |
ernstige agitatie (CMAI ≥35) |
113 (56/57)
|
4 wkn. |
CMAI; direct na afloop van behandeling en na 3 wkn. FU. |
3/6 |
|
Aromatherapie |
||||||||
|
Ballard, 2002 |
Citroenmelisse |
Instelling |
ernstig, CDR=3 |
dagelijkse agitatie met matige/ernstig problemen voor zorgpersoneel (NPI) |
72 (36/36) |
4 wkn. |
CMAI, NPI-agitatie |
4/6 |
|
Fu, 2013 |
Lavendel |
instelling |
MMSE≤24 (ernstig 29%, matig ernstig 37,7%, licht 14,7%); AD |
gedocumenteerde voorgeschiedenis, min. 14 dgn. (los of aaneengesloten) agitatie/agressie in afgelopen 3 mnd. |
45 (23/22)
|
6 wkn. |
CMAI-SF (short form); direct na afloop van interventie |
2/6 |
|
Lin, 2007 |
Lavendel |
instelling (care and attention home) |
diagnose dementie volgens DSM-IV; APA, 1994 |
klinisch sign. agitatie vastgesteld door onderzoekspsychiater met CMAI |
70 (35/35) |
3 wkn. |
CMAI & NPI |
3/6 |
|
Yang, 2015 |
Lavendel |
Instelling |
diagnose dementie door neuroloog of psychiater volgens DSM-IV |
ernstige agitatie (CMAI ≥35) |
130 (73/57)
|
4 wkn. |
CMAI; direct na afloop van behandeling en na 3 wkn. FU. |
3/6 |
|
O’Connor, 2013 |
Lavendel |
Instelling |
lichte dementie volgens Clinical Dementia Rating scale |
Fysiek geagiteerd gedrag op meerdere momenten per dag waarbij interventie van personeel nodig was. |
66 (38/28) |
1 week |
Gedragsobservaties (30 min.); Philadelphia Geriatric Center Affect Rating Scale; direct (0-30 en 30-60 min.) na afloop van therapie |
3/6 |
|
Burns, 2011 |
Citroenmelisse |
Instelling |
significante agitatie (CMAI>39 gedurende min. 4 wkn.) |
clinical dementia rating=3; NINCDS/ADRDA criteria for probable or possible Alzheimer’s disease |
77 (38/39) |
12 wkn. |
PAS; direct na afloop van interventie |
3/6 |
|
Mediatieve cognitief gedragstherapeutische interventies |
||||||||
|
Gormley, 2001 |
Gedragsmanagement programma mantelzorgers |
thuiswonend |
Dementie volgens ICD-10 |
Ten minste licht agressief beoordeeld door mantelzorger op globale item RAGE |
62 (34/28) |
8 wkn. |
RAGE |
3/6 |
|
Huang, 2003 |
Trainingsprogramma voor mantelzorgers |
Thuiswonend |
Diagnose dementia door psychiater of neuroloog |
CMAI≥50 |
59 (30/29) |
2 wkn. |
CMAI; nameting 3 wkn. en 3 mnd. na interventie |
3/6 |
|
Huang, 2013 |
Trainingsprogramma voor mantelzorgers |
thuiswonend |
Diagnose dementie; AD; VD |
CMAI≥50 |
129 (63/66) |
8 dgn. (2 sessies met 1 week ertussen) |
CMAI-fysiek agressief gedrag |
2/6 |
|
Wright, 2001 |
Verpleegkundig opleidings- en begeleidingsprogramma voor mantelzorgers |
thuiswonend |
AD |
Disrupted behaviors, opname in BICU |
93 (68/25) |
1 jr. |
CMAI |
3/6 |
|
McCallion, 1999 |
Family visit education program |
instelling |
Minimaal lichte dementie |
Probleemgedrag o.a. fysieke agressie, schelden, storende geluiden of motorische rusteloosheid |
66 (32/34) |
8 wkn. |
CMAI; meting na 3 en 6 mnd. |
4/6 |
|
Chenoweth, 2014 |
Persoonsgerichte zorg en omgeving |
instelling |
Diagnose dementie |
Beoordeeld op aanwezigheid van agitatie |
601 |
4 mnd. |
CMAI: direct na afloop en 8 mnd. FU |
4/6 |
|
Sloane, 2004 |
Trainingsprogramma persoonsgericht baden: Patiëntgericht douchen; Handdoekbad |
instelling |
MDS-COGS≥5; Diagnose Alzheimer of gerelateerde dementie |
Agitatie of agressie bij baden (≥3 episodes van agitatie/agressie in twee van drie baden; video, baseline) |
73 (49/24) |
6 wkn. |
CAREBA |
3/6 |
|
Visser, 2008 |
Staff education + peer support |
instelling |
dementie |
Regelmatig ≥1 gedraging uit CMAI |
76 |
8 wkn. |
CMAI; postinterventie, 3 en 6 mnd. FU |
2/6 |
|
Beck 2002 |
Gedragsinterventie (individueel) |
Instelling |
Mensen met matig ernstig tot ernstige dementie (MMSE <20) |
Gedragsontregelingen in de voorgaande 2 wkn. |
179 |
7 wkn. |
Disruptive behavior Scale; postinterventie en na 1 en 2 mnd. |
2/6 |
|
Overige interventies |
||||||||
|
Garland, 2007 |
Simulated presence |
instelling |
dementie |
Meerdere keren per dag geagiteerd gedrag in voorgaande 2 wkn (CMAI door personeel) |
30 |
4 wkn. |
Aanwezigheid van fysieke en verbale (niet)agressieve agitatie; 15 min tijdens interventie (data 15 min post interventie niet bruikbaar) |
2/6 |
|
Opie, 2002 |
Op persoon afgestemde multidisciplinaire interventie |
Instelling |
Dementie |
1 of meer keer per dag matig ernstige gedragsproblemen (CMAI door ervaren personeel |
99 |
4 wkn. |
CMAI en BAGS; 1 mnd. FU |
2/6 |
|
Kovach, 2004 |
Balancing Arousal Controls Excesses (BACE)
|
Instelling |
MMSE≤15; FAST 6-7 |
Identified by nurse as having some agitation |
102 (36/42)* |
1 week |
Observaties met VAS (elke 15 min. gedurende 12 uur); eerste dag van aangepast activiteitenschema |
3/6 |
|
Cohen-Mansfield, 2012 |
Treatment Route for Exploring Agitation (TREA) |
instelling |
dementie |
Meerdere keren per dag geagiteerd gedrag, volgens personeel |
125 (89/36) |
2 wkn. |
ABMI, laatste 3 dgn. van interventie |
3/6 |
1 Gescoord volgens de 6 domeinen van de Cochrane Risk of Bias tool 2.0 (score 0-6), waarbij een hogere score een hogere kwaliteit weergeeft en minder risico op bias en overschatting van het behandeleffect (zie tabblad ‘Verantwoording en methode’ voor details over deze beoordeling).
* Geen informatie over allocatie van uitvallers (n=24).
AD=Alzheimer dementie; VD= vasculaire dementie; CMAI=Cohen-Mansfield Agitation Inventory; PGCARS=Philadelphia Geriatric Center Affect Rating Scale; PAS= Pittsburgh Agitation Scale; FAST= Functional Assessment Staging Tool; CAREBA= Care Recipient Behavior Assessment; BICU= behavioral intensive care unit; RAGE=Rating Scale for Aggressive Behavior in the Elderly; ABMI= Agitation Behavior Mapping Instrument; BAGS= Behaviour Assessment Graphical System, FU = follow-up.
Resultaten en bewijskracht, symptomen van agitatie
Een overzicht van de resultaten en bewijskracht van de geïncludeerde RCT’s naar psychosociale en psychologische interventies voor geagiteerd gedrag bij mensen met dementie is weergegeven in het evidenceprofiel (zie tabel 2).
Activiteitentherapie
Effectiviteit van activiteitentherapie op symptomen van agitatie is onderzocht in drie RCT’s (Lin, 2009; Van der Ploeg, 2013; Buettner, 1996). Montessori-gebaseerde activiteitenprogramma’s zijn onderzocht in twee cross-over RCT’s (Lin, 2009; Van der Ploeg, 2013). In de cross-over RCT van Lin toont de GLMM-analyse met verschillende covariaten een significant effect van Montessori-activiteiten in vergelijking met de controle-interventie ‘aanwezigheid’ (β=-2,32; p<0,001. Ps: GLMM = Generalized Linear Mixed Model). De SMD (berekend op basis van de periode tot cross-over) toont een klein, niet significant effect, SMD= -0,35 [-0,77 tot 0,07]. De cross-over RCT van Van der Ploeg toont geen effect van gepersonaliseerde, een-op-een, Montessori-activiteiten op agitatie in vergelijking met niet-gepersonaliseerde activiteiten (CMAI-score: interventiegroep 17,6 (10,3) en controlegroep 17,0 (9,4); SMD= 0,06 [-0,56 tot 0,68]). Verpleeghuisbewoners die deelnamen aan het sensomotorisch activiteitenprogramma in de RCT van Buettner (1996) vertoonden in het algemeen niet meer of minder agitatie, gemeten met de CMAI, dan medebewoners die deelnamen aan een traditioneel activiteitenprogramma (p=0,08; geen data gerapporteerd om effectgrootte te berekenen). Tijdens de activiteiten was er minder agitatie, gemeten met de ‘Behavior section’ van het ‘Agitation behavior mapping instrument’, bij een sensomotorisch activiteitenprogramma vergeleken met het traditionele activiteitenprogramma (interventie=6,8; controle=14,0; p<0,01).
Muziekinterventie
Van de negen RCT’s naar effectiviteit van muziekinterventies voor agitatie bij 480 mensen met dementie, vonden zes RCT’s positieve effecten op agitatie (Garland, 2007; Gerdner, 2000; Sung, 2006; Ridder, 2013; Hicks-Moore, 2008; Remington, 2002). Groene (1993) vond geen verschil in agitatiesymptomen maar wel een toename van dwaalgedrag in de muziekinterventiegroep. De overige twee RCT’s vonden geen effect op geagiteerd gedrag (Cooke, 2010; Vink, 2012).
In de cross-over RCT van Cooke (2010) bij 47 deelnemers met lichte tot matig ernstige dementie die zeer licht geagiteerd gedrag vertoonden en verbleven in een zorginstelling, werd geen verschil gevonden in geagiteerd gedrag tussen de muziekinterventie (n=24) en de controle-interventie (n=23; lees- en sociale activiteiten) op de agitatie totaalscore (SMD= 0,01; 95% BI: -0,39 tot 0,42).
In de cross-over RCT van Gerdner (2000) bij 39 deelnemers met lichte tot ernstige dementie, bleek een individuele muziekinterventie de frequentie van geagiteerd gedrag significant te verminderen, vergeleken met een interventie met rustige klassieke muziek. Het betreft een matig groot effect (SMD= -0,73; 95% BI: -1,19 tot -0,27). Omdat geen data tot de cross-over beschikbaar waren, zijn data van de gehele duur van de RCT meegenomen.
In de RCT van Garland (2007) vertoonden deelnemers tijdens de individuele muziekinterventie significant minder frequent fysiek geagiteerd gedrag vergeleken met gebruikelijke zorg (MD= -0,81; p=0,04). Er is geen effect gevonden ten opzichte van andere auditieve prikkels aangeboden via een koptelefoon, namelijk de controle-interventie bestaande uit een neutraal geluidsfragment (MD= -0,53; p=0,09) of gesimuleerde aanwezigheid van naasten (zie overige interventies). Er was geen vermindering van verbaal geagiteerd gedrag tijdens de muziekinterventie in vergelijking met gebruikelijke zorg (MD=-0,53; p=0,10) of andere auditieve prikkels (controle-interventie (MD= 0,19; p=0,46) of gesimuleerde aanwezigheid van naasten (zie overige interventies)). Er is overigens wel een positief effect gevonden tussen de controle-interventie (neutraal geluidsfragment) en gebruikelijk zorg op verbale agitatie tijdens de interventie (MD=-0,73; p=0,03). Er zijn geen bruikbare gegevens gepresenteerd over agitatie na afloop van de interventie. Ook de effectgrootte kan niet worden berekend in verband met onvoldoende data.
In de RCT van Vink (2012) bij 77 deelnemers met lichte tot ernstige dementie die een uur voor de interventie geagiteerd gedrag vertoonden, werd geen meerwaarde aangetoond van de muziekinterventie in vergelijking met recreatieve activiteiten op geagiteerd gedrag (SMD kan niet worden berekend omdat data niet zijn gerapporteerd; p=0,09).
In de RCT van Sung (2006) bij 36 deelnemers met matige tot ernstige dementie in een zorginstelling werden positieve effecten van een gecombineerde muziek- en bewegingsinterventie aangetoond in vergelijking met gebruikelijke zorg. Direct na afloop van de interventie werd met de CMAI een statistisch significant matig groot effect in afname van geagiteerd gedrag gemeten in de interventiegroep (SMD= -0,70; 95% BI: -1,38 tot -0,02; p=0,001).
In de RCT van Groene (1993) bij 30 deelnemers met matig ernstige tot ernstige dementie was er geen verschil in nabij blijvend/zittend gedrag in de omgeving waar de sessie plaatsvond tussen patiënten die een muziekinterventie ontvingen (n=15) of de (voor)leesinterventie (SMD= -0,49; 95% BI: -1,22 tot 0,24; na de vijf sessies tot cross-over). Daarnaast was er een significant groot verschil in dwaalgedrag (afgelegde afstand/uur; zowel lopend als met rolstoel) ten nadele van deelnemers aan de muziekinterventie in vergelijking tot hen die deelnamen aan de leesinterventie (SMD= 1,13; 95% BI: 0,35 tot 1,91).
In de cross-over RCT van Ridder (2013) bij 42 deelnemers met matige tot ernstige dementie werd geen significante vermindering in de frequentie van geagiteerd gedrag waargenomen bij deelnemers aan de muziektherapie (en aanvullende activiteiten zoals wandelen of dansen) in vergelijking met gebruikelijke zorg (SMD= -0,21; 95% BI: -0,67 tot 0,26). Voor ernst van geagiteerd gedrag is een significant, matig effect gevonden ten gunste van de muziektherapie (SMD= -0,50; 95% BI: -0,93 tot -0,06).
In de RCT van Hicks-Moore (2008) bij 41 mensen met lichte tot matig ernstige dementie bleek het beluisteren van favoriete muziek in grote mate effectief in het verminderen van fysiek niet-agressief gedrag (SMD= –2,2; 95% BI –2,8 tot –1,6) en verbale agitatie (SMD= –1,0; 95% BI –1,5 tot –0,4) vergeleken met een controleconditie waar geen interventie plaatsvond. Er was geen significant verschil in fysiek agressief gedrag (SMD= –0,4; 95% BI –0,9 tot en met 0).
De RCT van Remington (2002) bij 34 mensen met voornamelijk matige of ernstige dementie in een instelling, rapporteerde een significant, groot effect op agitatie direct na afloop van de muziekinterventie (SMD= -1,40; 95% BI: -2,16 tot -0,64).
Zintuiglijke interventies
Van de acht RCT’s naar zintuiglijke interventies voor geagiteerd gedrag bij 430 mensen met dementie rapporteren vier RCT’s significant minder agitatie bij acupressuur (Lin, 2009), handmassage (Hicks-Moore, 2008; Remington, 2002) en acupressuur met aromatherapie (Yang, 2015). In de RCT van Hawranik (2008) verminderde de prevalentie van fysiek niet-agressief gedrag in zowel de therapeutisch aanraking en de gesimuleerde therapeutische aanraking als bij ten opzichte van gebruikelijke zorg. De overige drie RCT’s vonden geen effecten (Baillon, 2004; Fu, 2013; Moyle, 2014).
De RCT van Baillon (2004) vond geen significant verschil in agitatie tussen snoezelen en de controle-interventie (reminiscentie). Het verschil in agitatie (ABMI-score) tussen pre- en posttest was voor snoezelen -1,3 (IQR: -3,3 tot 3,0) en voor controle 0,8 (IQR: -1,6 tot 3,3).
Hawranik (2008) vond bij therapeutische aanraking (n=17) op de meting twee uur na de laatste sessie geen afname in fysiek agressief (SMD= 0,19; 95% BI: -0,47 tot 0,86), fysiek niet-agressief (SMD= -0,46; 95% BI: -1,13 tot 0,21) of verbaal geagiteerd gedrag (SMD= -0,63; 95% BI: -1,31 tot 0,06) ten opzichte van gebruikelijke zorg (n=18). In een analyse over de gehele vijfdaagse behandelperiode (zes metingen: vooraf en na elke van vijf sessies) was er wel een significant verschil gevonden tussen de groepen (therapeutische aanraking, gesimuleerde aanraking en gebruikelijke zorg) in fysiek niet-agressief gedrag (Χ2=5,89; p<0,05); de prevalentie van fysiek niet-agressief gedrag was in deze periode in de gebruikelijke zorggroep 2,3 keer hoger dan in de groep die therapeutische aanraking onderging (95% BI= 0,66 tot 7,81). Er zijn geen totaalscores van de behandelperiode beschreven.
In de cross-over RCT van Lin (2009) toonde de groep met de acupressuur significant minder geagiteerd gedrag in vergelijking met de controle-interventie. Dit blijkt uit zowel de eerste behandelperiode (SMD= -0,51; 95% BI: -0,93 tot -0,10) als uit de GLMM-analyse over de drie behandelperiodes van de trial (β=-2,11; SE=0,61; p=0,001).
In de cross-over RCT van Moyle (2014) nam in beide groepen (voetmassage versus rustige aanwezigheid) het geagiteerde gedrag toe. Deze toename was significant groter in de controlegroep (SMD= -0,63; 95% BI:-1,18; -0,07; p=0,03). Vanwege de toename van gedrag ook in de voetmassagegroep werd deze interventie in deze RCT als negatief/niet-effectief beschouwd.
De groep die handmassage ontving in de RCT van Remington (2002; n=34) toonde een significante, grote vermindering van geagiteerd gedrag, zowel in de tien minuten direct na afloop van de interventie (SMD= -1,41; 95% BI: -2,17 tot -0,64; p<0,05) als een uur nadien (SMD= -1,97; 95% BI: -2,81 tot -1,14; p<0,05).
De RCT van Hicks-Moore (2008) bij 41 mensen met lichte tot matig ernstige dementie toonde significante effecten van eenmalige handmassage in het verminderen van geagiteerd gedrag (ook wanneer gecombineerd met muziek) ten opzichte van een controleconditie waar geen interventie plaatsvond ter vermindering van geagiteerd gedrag. Het betrof een groot effect op fysiek niet-agressief gedrag (SMD= –1,4; 95% BI: –1,9 tot –0,8) en matig groot effect op verbale agitatie (SMD= –0,7; 95% BI: –1,3 tot –0,2). Er was geen verschil in fysiek agressief gedrag (SMD= –0,4; 95% BI: –0,9 tot 0,1). In deze RCT waren grote verschillen in baseline-agitatiescores tussen de handmassagegroep en de controlegroep.
In de RCT van Fu (2013; n=44) is geen verschil gevonden in agitatie tussen handmassage met aromatherapie en controle-interventie (waterspray zonder massage). Groepsdata zijn niet gerapporteerd waardoor de SMD niet berekend kan worden.
De RCT van Yang (2015; n=113) toont geen significante effecten van acupressuur met lavendelolie in vergelijking met gebruikelijke zorg (SMD= 0,19; 95% BI: -0,18 tot 0,56). Echter, de baselineverschillen waren groot en uit GEE-analyses blijkt een grote significante reductie in agitatie na acupressuur in verband met een toename in de controlegroep (posttest: Bèta = −15,31; 95% BI: −17,83 tot −12,79; p<0,01). Voor effecten van aromatherapie zonder acupressuur, zie aromatherapie (GEE analyse: Generalized Estimation Equation).
Aromatherapie
Zes RCT’s onderzochten de effectiviteit van aromatherapie op symptomen van agitatie bij 460 mensen met dementie. Vier RCT’s maakten gebruik van lavendelolie en twee van citroenmelisse.
Fu (2013) vond geen verschillen in agitatie tussen patiënten met lavendelolie-aromatherapie in vergelijking met de controle-interventie (waterspray; geen gegevens gerapporteerd).
Met gepaarde t-toetsen heeft Lin (2007) de voor- en nascores per arm vergeleken. In de lavendelgroep was er een afname van geagiteerd gedrag; de CMAI-score daalde van gem. 63,2 voor de interventie naar gem. 58,8 na de interventie (p<0,001). In de controlegroep was er geen afname van geagiteerd gedrag zichtbaar; de CMAI-score in deze groep bleef nagenoeg gelijk 63,9 (p=0,52). Lin heeft de twee groepen niet direct met elkaar vergeleken. Berekening van de effectgrootte toonde een kleine, niet significante afname van agitatie bij gebruik van lavendelolie (SMD= -0,29; 95% BI: -0,77 tot 0,18).
Hoewel de GEE-analyse (generalized estimating equations) voor herhaalde metingen van Yang (2015) een significante afname toont van CMAI-scores in de nameting en na drie weken follow-up (p=0,01), worden deze verschillen (grotendeels) verklaard door baselineverschillen. De agitatie in de lavendelgroep blijft nagenoeg gelijk; van 41,8 in de voormeting, naar 41,1 en 39,8 in de nameting en de follow-up. Dit komt ook naar voren in de SMD. Deze toont een zeer klein, niet significant effect van aromatherapie met lavendel in vergelijking met gebruikelijke zorg (SMD= -0,09; 95% BI: -0,44 tot 0,26).
O’Connor (2013) vond geen significant behandeleffect van lavendelolie versus placebo-olie op geagiteerd gedrag in de dertig minuten observatie direct na afloop van de interventie (SMD= -0,14; 95% BI: -0,64 tot 0,36) als in het tweede half uur na de interventie (SMD= -0,10; 95% BI: -0,60 tot 0,39).
In de RCT van Burns (2011) was geen significante vermindering van symptomen van agitatie na aromatherapie met citroenmelisse ten opzichte van de controle (SMD kan niet berekend worden vanwege zeer scheve verdeling van de PAS-data; mediaan PAS-score en range interventiegroep = 1,3 (0-14) en controlegroep = 1,7 (0-16)).
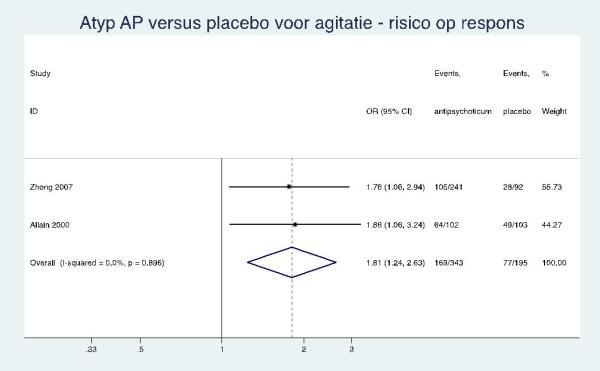
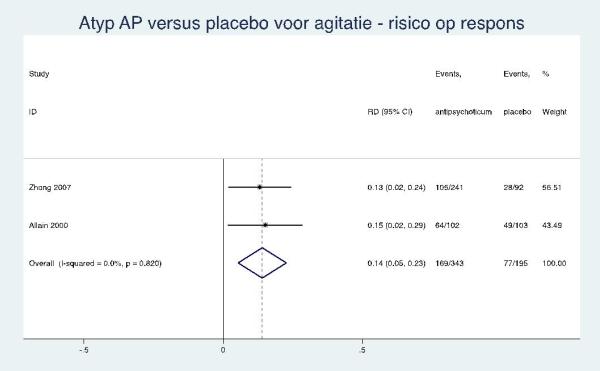
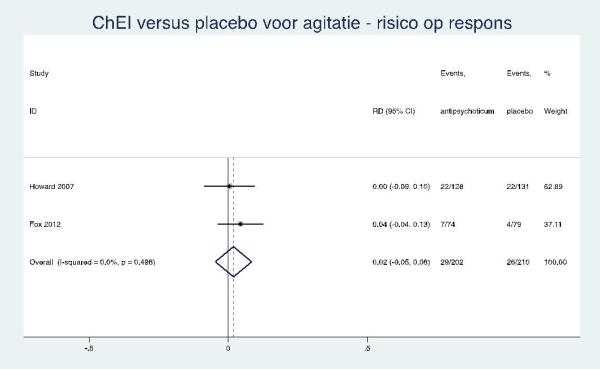
De effectgrootte in de RCT van Ballard (2002) naar citroenmelisse toonde een kleine, niet significante vermindering van agitatie bij aromatherapie met citroenmelisse, gemeten met de CMAI-totaalscore vergeleken met een controle-interventie (SMD= -0,44; 95% BI: -0,91 tot 0,03). De CMAI-scores zijn echter zeer scheef verdeeld. Daarom toetsen de auteurs de verschilscores (verschil in CMAI-score tussen voor- en nameting) van de citroenmelissegroep en controlegroep met een non-parametrische ‘Mann-Whitney-U-toets’. Hoewel de agitatie in beide groepen significant daalde (Wilcoxon Z-toets), was er een grotere daling van agitatie in de citroenmelissegroep vergeleken met de controlegroep (p<0,001). Ballard (2002) rapporteerde ook het percentage patiënten dat een klinisch relevante respons vertoonde. Aromatherapie met citroenmelisse gaf in de groep met aromatherapie significant meer patiënten met een klinisch relevante respons (>30% verbetering op CMAI; I=21/35; C=5/36; OR= 9,30; 95% BI: 2,91 tot 29,72).
Mediatieve cognitieve gedragstherapie
Gormley (2001), Wright (2001) en Huang (2003 & 2013) onderzochten de effectiviteit van mediatieve interventies voor geagiteerd gedrag bij mensen met dementie die thuis verblijven.
Uit de RCT van Gormley (2001) blijkt het gedragsmanagementprogramma voor mantelzorgers van thuiswonende ouderen met dementie geen significant effect te hebben op agressief gedrag van hun naaste (SMD= -0,42; 95% BI: -0,92 tot 0,09). Ook de RCT van Wright (2001) vindt geen significant effect van het eenjarig opleidings- en begeleidingsprogramma voor mantelzorgers op agitatie van hun thuiswonende naasten (geen data gerapporteerd).
De RCT’s van Huang onderzochten effecten van een trainingsprogramma voor mantelzorgers op geagiteerd (Huang, 2003) en agressief gedrag (Huang, 2013) van hun naaste. In 2003 vond Huang op de nameting geen verschil tussen het trainingsprogramma voor mantelzorgers op agitatie (CMAI-totaalscore) van hun naasten (SMD= -0,04; 95% BI: -0,60 tot 0,53). Echter, de auteurs vermelden dat de GEE-analyse wel een significant verschil toonde wanneer rekening werd gehouden met de verschillen op baseline. Cijfers van deze GEE-analyse zijn niet gepubliceerd.
In de RCT van Huang uit 2013 naar het trainingsprogramma voor mantelzorgers werd twee weken na afloop van de interventie niet significant minder vaak agressief gedrag vertoond in de interventiegroep (OR= 0,47; 95% BI: 0,21 tot 1,06; Χ2-toets: p=0,06). Na drie maanden was er wel sprake van significant minder patiënten met fysiek agressief gedrag (OR= 0,28; 95% BI: 0,10 tot 1,76; Χ2-toets: p=0,01), maar het effect was in de meting na zes maanden verdwenen (OR= 0,62; 95% BI: 0,25 tot 1,55; Χ2-toets: p=0,20).
De effectiviteit van mediatieve interventies tegen agitatie bij verpleeghuisbewoners is onderzocht door McCallion (1999), Chenoweth (2014), Sloane (2004), Visser (2008) en Beck (2002).
In de RCT McCallion (1999) naar effectiviteit van het ‘Family visit education program’ zijn op twee momenten (na drie maanden en na zes maanden) drie CMAI-subschaalscores (fysieke agressie, fysiek niet-agressief en verbaal geagiteerd) gerapporteerd door twee verschillende observatoren. Zowel de SMD’s als de toetsing met random regressiemodellen tonen op geen van de zes uitkomsten (2 observatoren x 3 schaalscores) een significant verschil in geagiteerd gedrag bij de posttestmeting na drie maanden. De effectgroottes (SMD) varieerden tussen -0,06 (95% BI: -0,54 tot 0,0,43) en -0,41 (95% BI: -0,89 tot 0,08). De toetsing met random regressiemodellen over de periode van baseline tot de tweede nameting na zes maanden na de interventie toonde bij twee van de zes gerapporteerde resultaten een significant interactie-effect tussen behandeling en tijd. Het betrof verbaal geagiteerd gedrag tijdens het familiebezoek gedurende een periode van twintig minuten (p<0,005) en fysiek niet-agressief gedrag gedurende de afgelopen twee weken (p<0,001) ten gunste van de ‘Family visit education interventie’.
De effectiviteit van persoonsgerichte zorg en een persoonsgerichte omgeving op geagiteerd gedrag bij bewoners met dementie is door Chenoweth (2014) onderzocht in een vierarmige trial. De nameting toonde geen effect van ‘op de persoon afgestemde zorg’ en/of ‘op de persoon afgestemde omgeving’ vergeleken met gebruikelijke zorg en omgeving. De SMD’s zijn verwaarloosbaar klein en niet significant verschillend (Chenoweth’s, 2014). De paarsgewijze vergelijkingen met behulp van GLMM tonen echter een significant effect voor ‘op de persoon afgestemde omgeving’. Dit wordt waarschijnlijk veroorzaakt door de relatief grote verschillen op baseline (regressie naar het gemiddelde). Voor de ‘op de persoon afgestemde zorg’ en de combinatie van op de persoon afgestemde zorg en omgeving toont ook deze analyse geen significant effect (persoonsgerichte zorg vs. controle: SMD= 0,08 [-0,14 tot 0,31]; GLMM-analyse p=0,06; persoonsgerichte omgeving vs. controle: SMD= 0,03 [-0,19 tot 0,26]; GLMM-analyse p=0,04; persoonsgerichte zorg + omgeving vs. controle: SMD= 0,12 [-0,11 tot 0,35]; GLMM-analyse: p=0,41).
In de RCT van Sloane (2004) zijn tijdens de badinterventies 'patiëntgericht douchen' en het 'handdoekbad' minder agitatie en agressie gerapporteerd in vergelijking met douchen zonder patiëntgerichte training (resp. SMD= -0,38; 95% BI: -0,89 tot 0,12 en SMD= -0,52; 95% BI: -1,03 tot -0,01). Waarschijnlijk geeft de zeer scheve verdeling van de data een vertekend beeld. De auteurs maken daarom gebruik van de parametrische ‘Wilcoxon rangsomtoets’ voor het vergelijken van de verschilscores tussen interventie en controle. Deze analyses tonen significante verschillen in verschilscores tussen patiëntgericht douchen en controle (p=0,02) en tussen handdoekbad en controle (p=0,01). Er is geen verschil tussen beide interventies.
In de RCT van Visser (2008) naar behandeleffecten van opleiden van personeel met of zonder peer support op agitatie van bewoners zijn geen significante groeps-, tijd- of interactie-effecten gevonden tussen pre- en posttestscores op de subschalen fysiek niet-agressief, fysiek agressief, verbaal niet-agressief en verbaal agressief gedrag (CMAI-totaalscores zijn niet gerapporteerd).
In de RCT van Beck (2002) werden geen significante verschillen gevonden tussen een van de interventies (ADL-interventie; psychosociale activiteiten (PSA); of deze gecombineerd) en gebruikelijke zorg op gedrag gemeten met de disruptive behavior scale (ADL-interventie, SMD= -0,40; 95% BI: -0,99 tot 0,19; PSA, SMD= 0,05; 95% BI: -0,52 tot 0,63; gecombineerde interventie, SMD= 0,01; 95% BI: -0,60 tot 0,62).
Overige interventies
Bij de vier RCT’s naar overige interventies bij 360 deelnemers met dementie, werden in twee RCT’s significante verbetering in agitatie gezien in vergelijking met een controle-interventie (Kovach, 2004; Cohen-Mansfield, 2012). In de andere twee RCT’s verminderde het geagiteerde gedrag in alle groepen (Garland, 2007; Opie, 2002).
In de RCT van Garland (2007) bleek een interventie met per koptelefoon gesimuleerde aanwezigheid van familie effectief in het verminderen van frequentie van fysiek geagiteerd gedrag met 30% (p=0,003) (MD = -0,96) en verbaal geagiteerd gedrag met 33% (p=0,04)(MD= -1,12). Echter, bleek ook de muziekinterventie en de controle-interventie met een neutraal voorgelezen geluidsfragment significant effectiever dan gebruikelijke zorg (resp. 25% vermindering van verbaal geagiteerd gedrag; p=0,04; en 29% vermindering van verbaal geagiteerd gedrag; p= 0,03).
In de RCT van Opie (2002) kregen de meeste bewoners een combinatietherapie (94%) en werden de data van de verschillende gecombineerde interventies niet apart gepresenteerd. Het deel van de trial dat als RCT werd aangemerkt, toonde geen significante verschillen tussen de interventiegroep en de ‘wachtlijst’-groep op frequentie van geagiteerd gedrag. In beide groepen werd voorafgaand aan de interventie al een daling in gedragsproblemen waargenomen. De ‘Behaviour assessment graphical system-metingen’ toonden geen verbeteringen in beide groepen op rusteloosheid, verbale agitatie, ongepast gedrag en totaalscore voor gedragsproblemen.
De BACE-interventie (Kovach, 2004), waarbij de aangeboden activiteiten een optimale balans in arousal moesten bevorderen, werd geen significante verbetering in agitatie bereikt (SMD= -0,09; 95% BI: -0,54 tot 0,35; p=0,43). Wanneer echter werd gecontroleerd voor baseline verschillen in arousal disbalans, werd een significant effect gevonden op agitatie ten gunste van de BACE-interventiegroep (p<0,05).
Cohen-Mansfield (2012) vond in haar RCT naar de ‘Treatment route for exploring agitation-methode’(TREA-methode) voor het op maat aanbieden van interventies in verpleeghuizen, dat er een significant verschil was ten gunste van de interventie (SMD= -1,08; 95% BI: -1,49 tot -0,67). Er werden geen nadelige effecten gemeld.
Resultaten en bewijskracht, bijwerkingen
Bijwerkingen aromatherapie
Vier RCT’s rapporteren dat er geen bijwerkingen zijn geconstateerd (O’Connor, 2013; Fu, 2013; Yang, 2015; Lin, 2007). Van de andere drie RCT’s rapporteert een RCT één persoon met twee dagen diarree in de interventiegroep (Ballard, 2002; OR= 3,08; 95% BI: 0,12 tot 78,27) en een andere RCT rapporteert een gelijk aantal ‘serious adverse events’ in de groep met citroenmelisse of placebo (Burns, 2011; OR= 1,00; 95% BI 0,13 tot 7,59).
Tabel 2. Evidenceprofiel over psychologische en psychosociale interventies voor geagiteerd gedrag bij mensen met dementie
|
Uitkomstmaat |
Trials (N)
|
Kwaliteit van het bewijs |
n per groep |
Behandeleffecten† |
Algemene beoordeling |
|||||||||||||
|
Vertekend1 |
Inconsi-stent |
Indirect |
Niet precies2 |
Publica-tiebias |
I |
C |
SMD of OR [95%BI] |
|||||||||||
|
Activiteitentherapie |
||||||||||||||||||
|
Agitatie (symptomen) |
3 |
Ja |
Ja |
Nee |
Ja |
Nee |
70/78 |
97/106 |
|
Zeer laag |
||||||||
|
Van der Ploeg, 2013 |
|
|
|
|
|
|
15/21 |
29/36 |
SMD= 0,06 [-0,56; 0,68] |
|
||||||||
|
Lin, 2009 |
|
|
|
|
|
|
39/39 |
52/52 |
SMD= -0,35 [-0,77 tot 0,07] GLMM-analyse met covariaten β=-2,32; p<0,001. |
|
||||||||
|
Buettner, 1997 |
|
|
|
|
|
|
16/18 |
16/18 |
Algemene agitatie (CMAI) alleen p-waarde gerapporteerd, p<0,08. Agitatie tijdens activiteiten ABMI-Behavior interventie=6,78; controle=14,0; p<0,01 |
|
||||||||
|
Uitval |
1 |
Ja |
Ja |
Nee |
Ja |
Ja |
|
|
|
Zeer laag |
||||||||
|
Van der Ploeg, 2013 |
|
|
|
|
|
|
3/21 |
1/36 |
OR= 5,83 [0,57; 60,16] |
|
||||||||
|
Muziekinterventies |
||||||||||||||||||
|
Agitatie symptomen |
9 |
ja |
ja |
nee |
Ja |
nee |
256 |
224 |
|
Zeer laag |
||||||||
|
Sung, 2006 |
|
|
|
|
|
|
18/20 |
18/20 |
SMD= -0,70 [-1,38; -0,02] |
|
||||||||
|
Groene, 19931 |
|
|
|
|
|
|
15 |
15 |
SMD= -0,49 [-1,22; 0,24] |
|
||||||||
|
Groene, 19931; Dwaalgedrag |
|
|
|
|
|
|
15 |
15 |
SMD= 1,13 [0,35; 1,91] |
|
||||||||
|
Ridder, 2013; Ernst geagiteerd gedrag |
|
|
|
|
|
|
38/42 |
39/42 |
SMD= -0,50 [-0,93; -0,06] |
|
||||||||
|
Ridder, 2013; Frequentie geagiteerd gedrag |
|
|
|
|
|
|
38/42 |
39/42 |
SMD= -0,21 [-0,67; 0,26] |
|
||||||||
|
Hicks-Moore, 2008 |
|
|
|
|
|
|
32 |
9 |
SMD fysiek niet-agressief gedrag= –2,2 [–2,8; –1,6]; SMD verbale agitatie= –1,0 [–1,5; –0,4] SMD fysiek agressief gedrag= –0,4 [–0,9; 0] |
|
||||||||
|
Remington, 2002 |
|
|
|
|
|
|
17 |
17 |
SMD= -1,40 [-2,16; -0,64] |
|
||||||||
|
Vink, 2013 |
|
|
|
|
|
|
43 |
34 |
F= 2,89; p=0,09 |
|
||||||||
|
Cooke, 2010 |
|
|
|
|
|
|
24 |
23 |
SMD= 0,01 [-0,39; 0,42] |
|
||||||||
|
Garland, 2007 |
|
|
|
|
|
|
30/74 |
30/74 |
Fysieke agitatie MD interv vs. gebruikelijke zorg=0,81, p=0,04 Verbale agitatie MD interv vs. gebruikelijke zorg= 0,53; p=0,10 |
|
||||||||
|
Gerdner, 2000 |
|
|
|
|
|
|
39 |
39 |
SMD= -0,73 [-1,19; -0,27] |
|
||||||||
|
Uitval |
3 |
ja |
ja |
nee |
Ja |
nee |
|
|
|
Zeer laag |
||||||||
Zoeken en selecteren inzet lichttherapie
Gevonden RCT’s
Er werd één meta-analyse en er werden tien RCT’s op volledige tekst beoordeeld. Daarvan voldeden vier RCT’s aan de selectiecriteria (Burns, 2009; Ancoli-Israel, 2003 a/b; Lyketsos, 1999; NCT02686190). Deze laatste was een ongepubliceerde RCT (https://ClinicalTrials.gov/show/NCT02686190). Hiervan waren nog geen resultaten beschikbaar, bleek na contact met de hoofdonderzoeker. De geëxcludeerde RCT’s zijn weergegeven in de exclusietabel in bijlage 2.1.
Samenvatting literatuur inzet lichttherapie
Kenmerken en kwaliteit van geïncludeerde RCT’s naar lichttherapie voor geagiteerd gedrag bij mensen met dementie
Drie RCT’s waarin de effectiviteit van lichttherapie met volledig spectrum werd onderzocht bij mensen met agitatie, konden worden geïncludeerd. De intensiteit varieerde van 2.500 tot 10.000 lux en daarbij verschilden ook de momenten waarop lichttherapie werd gegeven, in de ochtend en/of aan het eind van de dag. De RCT’s werden uitgevoerd bij 15 tot 92 patiënten met dementie en effectiviteit werd gemeten met de CMAI of BEHAVE-AD. Een overzicht van de kenmerken en kwaliteit van de geïncludeerde RCT’s naar psychofarmaca voor geagiteerd gedrag bij mensen met dementie, is weergegeven in Tabel 3. Er was een matig tot hoog risico op bias, zie risk-of-biastabel in bijlage 2.2.
Tabel 3. Kenmerken en kwaliteit van geïncludeerde RCT’s naar lichttherapie voor geagiteerd gedrag bij mensen met dementie
|
Publicatie |
Licht (intensiteit; spectrum) |
Blootstelling (duur) |
|
Setting |
Dementie1 (ernst; type) |
Agitatie2 (ernst; criteria) |
N |
Trial-duur |
Meet-instrument2 |
Kwaliteit opzet en uitvoering3 |
|
Burns, 2009 |
10.000 lux; full spectrum |
2 uur/dag |
|
instelling |
licht - ernstig |
CMAI |
48 |
8 wkn. |
CMAI |
3/6 |
|
Ancoli-Israel, 2003 |
2500 lux; full spectrum |
2 uur/dag |
|
instelling |
ernstig; AD |
CMAI |
92 |
1,5 week |
CMAI |
2/6 |
|
Lyketsos, 1999 |
10.000 lux; full spectrum |
1 uur/dag |
|
instelling |
ernstig; AD/VaD |
BEHAVE-AD |
15 |
4 wkn |
BEHAVE-AD |
2/6 |
CMAI: Cohen-Mansfield Agitation Inventory; BEHAVE-AD: Behavioral Pathology in Alzheimer’s Disease Rating Scale.
Resultaten en bewijskracht over effectiviteit van lichttherapie voor geagiteerd gedrag bij mensen met dementie
Tabel 4 toont het evidenceprofiel met de resultaten en bewijskracht over effectiviteit van de geïncludeerde RCT’s.
De drie RCT’s die zijn geïncludeerd rapporteerden geen poolbare resultaten. Resultaten van twee van de RCT’s (Ancoli-Israel, 2003a/b & Burns, 2009) zijn wel gevonden in een meta-analyse over lichttherapie bij mensen met dementie (Forbes, 2014). Deze gegevens zijn gebruikt met als resultaat een niet-significant, klein effect (SMD= 0,148 (95% BI: -0,226 tot 0,523). Dit is in lijn met de resultaten van de derde RCT, waarin vijf van de vijftien participanten stopten met lichttherapie vanwege een toename van de agitatie (Lyketsos, 1999). Het was onduidelijk in welke fase dit gebeurde, voor of na cross-over.
Resultaten en bewijskracht over bijwerkingen van lichttherapie voor geagiteerd gedrag bij mensen met dementie
Geen van de drie geïncludeerde RCT’s vermeldden of en welke bijwerkingen er waren als lichttherapie gegeven werd voor agitatie bij mensen met dementie.
Resultaten en bewijskracht over uitval
De drie geïncludeerde RCT’s vermeldden de uitval in de behandelgroepen niet.
Tabel 4. Evidenceprofiel voor lichttherapie bij geagiteerd gedrag bij mensen met dementie
|
Uitkomst |
N trials |
Kwaliteit van het bewijs |
n1/ N per groep |
Behandeleffecten |
Algemene beoordeling |
|||||||
|
Vertekend2 |
inconsistent |
indirect |
Niet precies3 |
Publicatie bias |
medicatie |
placebo |
SMD3 [95% BI] |
OR [95% BI] |
ARR4 [95% BI] |
|||
|
symptomen |
2 |
ja |
nee |
nee |
ja |
nee |
60/60 |
49/49 |
0,15 [-0,23; 0,52] |
|
|
laag |
|
klinisch relevante respons |
0 |
|
|
|
|
|
|
|
|
|
|
|
|
≥1 bijwerkingen |
0 |
|
|
|
|
|
|
|
|
|
|
|
|
Uitval |
0 |
|
|
|
|
|
|
|
|
|
|
|
Zoeken en selecteren inzet psychofarmaca
Gevonden RCT’s
Er werden 26 meta-analyses, 74 RCT’s en twee protocollen op volledige tekst beoordeeld. Daarvan voldeden 22 RCT’s aan de selectiecriteria, waarin meestal in twee en soms in drie armen de volgende middelen werden onderzocht: klassieke antipsychotica (Allain, 2000; Auchus, 1997; Teri, 2000), atypische antipsychotica (Zhong, 2007; Ballard, 2005; Allain, 2000; Brodaty, 2003), antidepressiva (Porsteinsson, 2014; Teri, 2000; Auchus, 1997), anti-epileptica (Olin, 2001; Tariot, 1998; Sommer, 2009; Porsteinsson, 2001), en antidementiemiddelen (Howard, 2007; Burns, 2011; Herrmann, 2013; Fox, 2012; Ballard, 2005). De geëxcludeerde RCT’s staan in de exclusietabel in bijlage 3.1.
Samenvatting literatuur inzet psychofarmaca
Kenmerken en kwaliteit van geïncludeerde RCT’s
Tabel 5 geeft een overzicht van de kenmerken en kwaliteit van de geïncludeerde RCT’s naar psychofarmaca voor geagiteerd gedrag bij mensen met dementie.
Klassieke antipsychotica
Drie RCT’s met haloperidol in doses van 0,5 tot 6 mg konden worden geïncludeerd. Twee daarvan werden uitgevoerd bij thuiswonende patiënten met de ziekte van Alzheimer, en de derde bij mensen met ziekte van Alzheimer, vasculaire dementie of een mengbeeld in het verpleeg-of ziekenhuis. Ernst van de dementie varieerde tussen licht en ernstig; de definitie van agitatie verschilde per RCT (volgens de subschaal ‘Agitatie’ van de ‘Multidimensional observation scale for elderly subjects’ (MOSES), de CMAI, of de mantelzorger). Ook in omvang (twaalf tot 204 patiënten) en duur (drie tot zestien weken) waren de RCT’s verschillend. Agitatie werd gemeten met de MOSES of de CMAI. Het risico op bias was zeer hoog bij de kleinste en grootste RCT en redelijk hoog bij de middelgrote RCT.
Atypische antipsychotica
Twee RCT’s onderzochten quetiapine in doses tussen 50 en 200 mg per dag bij 62 en 333 verpleeghuispatiënten met matig tot ernstige ziekte van Alzheimer of vasculaire dementie. De duur van deze RCT’s was respectievelijk zes en tien weken. Agitatie werd gemeten met behulp van de CMAI en de ‘Positive and negative syndrome scale - excitement component’ (PANNS-EC). Ook is er een RCT met 100 tot 300 mg tiapride bij patiënten met lichte tot matige ziekte van Alzheimer, vasculaire dementie of en mengbeeld die waren opgenomen in een verpleeghuis of ziekenhuis. Een subscore van de MOSES werd gebruikt om agitatie te meten. In elk van deze RCT’s was het risico op bias zeer hoog.
Tot slot is er een RCT met risperidon voor agressie bij verpleeghuispatiënten met matige tot ernstige ziekte van Alzheimer, vasculaire dementie of gemengde vorm. Patiënten met alleen niet-agressieve vormen van agitatie waren uitgesloten. De duur van de RCT was twaalf weken en de dosis van risperidon varieerde tussen 0,5 en 2mg per dag. Agressie werd gemeten met de betreffende subschaal van de CMAI. Ook deze trial had een hoog risico op bias.
Antidepressiva
Er konden drie RCT’s worden geïncludeerd, waarvan twee met SSRI’s en één met trazodon, vallend onder de ‘overige antidepressiva’. Alle RCT’s werden uitgevoerd bij patiënten met de ziekte van Alzheimer. De grootste RCT was met 30 mg citalopram bij 186 patiënten gedurende negen weken. Ook was er een RCT met gemiddeld 200 mg trazodon bij 73 thuiswonende patiënten van zestien weken. En er was een RCT met 20 mg fluoxetine bij twaalf thuiswonende patiënten. Effectiviteit op agitatie werd steeds gemeten met de CMAI. Het risico op bias varieerde van matig tot zeer hoog.
Anti-epileptica
Er waren vijf RCT’s met anti-epileptica, waarvan twee met carbamazepine in een dosis van 300 tot 400 mg, één met 300 tot 900 mg oxcarbazepine en twee met 375 tot 1375 mg valproaat. Met uitzondering van een carbamazepine-RCT in de thuissituatie, waren deze RCT’s uitgevoerd bij verpleeghuispatiënten. De ernst en het type dementie verschilde per RCT; de omvang van de studiepopulatie varieerde tussen 21 en 153. De duur voor de meeste RCT’s was zes weken, de oxcarbazepine RCT duurde acht weken. Effectiviteit op agitatie werd gemeten met de BPRS-agitatie, de CGIC of de ‘NPI-NH agitatie subschaal’. Het risico op bias varieerde van redelijk tot zeer hoog (CGIC= Clinical Global Impression Scale)
Antidementiemiddelen
Er waren vijf RCT’s met antidementiemiddelen: twee met donepezil (10 respectievelijk 20 mg), twee met 20 mg memantine en één met 9 mg rivastigmine. Alle RCT’s werden uitgevoerd bij mensen met de ziekte van Alzheimer, maar in ernst en setting waren ze variabel. Agitatie werd gediagnosticeerd aan de hand van de CMAI en/of de ‘NPI agitatie subschaal’. Populaties waren redelijk groot (variërend van 62 tot 369 patiënten) en de duur was tussen de zes en 24 weken. Effectiviteit werd gemeten met de CMAI, de NPI agitatie subschaal of de PAS. De RCT’s scoorden een hoog risico op bias, met uitzondering van een van de RCT’s naar memantine.
Tabel 5. Kenmerken en kwaliteit van geïncludeerde RCT’s naar psychofarmaca voor geagiteerd gedrag bij mensen met dementie
|
Publicatie |
Medicijn |
Dosis |
Setting |
Dementie (ernst; type)1 |
Agitatie (ernst; criteria)2 |
N |
Trialduur, weken |
Meetinstrument2 |
Kwaliteit opzet en uitvoering3 |
|
Klassieke antipsychotica |
|||||||||
|
Allain 2000 |
haloperidol |
2- 6 mg |
instelling |
licht - matige; AD, VaD, of mixed |
MOSES prikkelbaarheid/agressiviteit subscore |
204 |
3 |
MOSES prikkelbaarheid/agressiviteit subscore |
2/6 |
|
Auchus 1997 |
haloperidol |
3 mg |
thuis |
AD4 |
CMAI |
12 |
6 |
CMAI |
1/6 |
|
Teri 2000 |
haloperidol |
0,5 – 3 mg (gemiddeld 1,8 mg) |
thuis |
matig - ernstig; AD |
opinie mantelzorger |
70 |
16 |
CMAI |
4/6 |
|
Atypische antipsychotica |
|||||||||
|
Zhong 2007 |
quetiapine |
100 of 200 mg |
instelling |
matig - ernstig; AD of VaD |
PANSS-EC |
333 |
10 |
PANSS-EC |
1/6 |
|
Ballard 2005 |
quetiapine |
50 – 100 mg |
instelling |
meesten ernstig; AD |
CMAI en NPI |
62 |
6 |
CMAI |
1/6 |
|
Allain 2000 |
tiapride |
100 – 300 mg |
instelling |
licht - matig; AD, VaD, of mixed |
MOSES prikkelbaarheid/agressiviteit subscore |
205 |
3 |
MOSES prikkelbaarheid/ agressiviteit subscore |
1/6 |
|
Brodaty 2003 |
risperidon |
Flexibel, 0,5 tot 2mg |
instelling |
matig - ernstig; AD VaD, of mixed |
CMAI-agressie subschaal |
345 |
12 |
CMAI-agressie subschaal |
0/6 |
|
Antidepressiva |
|||||||||
|
Porsteinsson 2014 (CitAD) |
citalopram |
30 mg |
NG |
licht - ernstig; AD |
NPI |
186 |
9 |
CMAI |
3/6 |
|
Teri 2000 |
trazodon |
50 – 300 mg (gemiddeld 200 mg) |
thuis |
matig - ernstig; AD |
opinie mantelzorger |
73 |
16 |
CMAI |
4/6 |
|
Auchus 1997 |
fluoxetine |
20 mg |
thuis |
licht - ernstig; AD |
CMAI |
12 |
6 |
CMAI |
1/6 |
|
Anti-epileptica |
|||||||||
|
Olin 2001 |
carbamazepine |
400 mg |
thuis |
ernstig; AD |
BPRS + geen baat bij antipsychotica |
21 |
6 |
CGIC |
1/6 |
|
Tariot 1998 |
carbamazepine |
flexibel, gemiddeld 300 mg |
instelling |
ernstig; AD, VaD, mix |
BPRS |
51 |
6 |
BPRS agitatie |
3/6 |
|
Sommer 2009 |
oxcarbazepine |
300 – 900 mg |
instelling |
matig - ernstig; AD/VaD |
NPI-NH |
103 |
8 |
NPI-NH agitatie |
4/6 |
|
Tariot 2005 |
valproaat |
750 mg |
instelling |
licht - ernstig; AD |
BPRS |
153 |
6 |
BPRS agitatie |
3/6 |
|
Porsteinsson 2001 |
valproaat |
375 – 1375 mg |
instelling |
ernstig; AD/VaD/mix |
BPRS |
56 |
6 |
BPRS agitatie |
3/6 |
|
Antidementiemiddelen |
|||||||||
|
Howard 2007 (CALM-AD) |
donepezil |
20 mg |
instelling + thuis |
ernstig; AD |
CMAI |
259 |
12 |
CMAI |
2/6 |
|
Burns 2011 |
donepezil |
10 mg |
instelling |
ernst NG; AD |
CMAI |
76 |
12 |
PAS |
2/6 |
|
Herrmann 2013 |
memantine |
20 mg |
thuis |
matig – ernstig; AD |
NPI-agitatie subscore |
369 |
24 |
CMAI |
2/6 |
|
Fox 2012 |
memantine |
20 mg |
instelling |
matig – ernstig; AD |
CMAI |
153 |
12 |
CMAI |
4/6 |
|
Ballard 2005 |
rivastigmine |
9 mg |
instelling |
meesten ernstig; AD |
CMAI en NPI |
62 |
6 |
CMAI |
2/6 |
1 AD: ziekte van Alzheimer; VaD: vasculaire dementie; NG: niet gerapporteerd
2 PANSS-EC: Positive and Negative Syndrome Scale-Excitement Component, 5 items, range 5 tot 35, [GtN1] hogere score betekent meer agitatie (Lindenmayer 2004).
MOSES prikkelbaarheid/agressiviteit subscore: range tot 40, waarbij een hogere score meer prikkelbaarheid/agressiviteit betekent (Helmes 1988).
BPRS: Brief Psychiatric Rating Scale, 18 items, range 0 tot 108, hogere score betekent ernstiger psychiatrische symptomen (Beller 1984).
PAS: Pittsburgh Agitation Scale, 16 items, range 0 tot 16 (Rosen 1994)
NPI agitatie/agressie: 1 item uit de Neuropsychiatric Inventory, range 0 tot 12, waarbij een hogere score staat voor meer en/of vaker agitatie/agressie (Iverson 2002).
CMAI: Cohen-Mansfield Agitation Index, 29 items, range 29 tot 203, hogere score betekent meer agitatie (Cohen-Mansfield 1989).
CGIC: Clinical Global Impression of Change (CGIC), waarbij respons wordt geduid als verbetering of verslechtering ten opzichte van baseline (Guy 1976).
3Gescoord volgens de 6 domeinen van de Cochrane Risk of Bias tool 2.0 (score 0-6), waarbij een hogere score een hogere kwaliteit weergeeft, minder risico op bias en overschatting van het behandeleffect (zie tabblad ‘Verantwoording en methode’ voor details over deze beoordeling).
Resultaten en bewijskracht over effectiviteit van medicatie
Tabel 6 toont het Evidenceprofiel met de resultaten en bewijskracht over de effectiviteit van de onderzochte middelen. De forest plots worden weergegeven in bijlage 3.3.
Klassieke antipsychotica
Data over effectiviteit van haloperidol kon van twee van de drie RCT’s gebruikt worden voor meta-analyses (Auchus 1997 als uitzondering). Deze analyse toonde een SMD van -0,36 (95% BI: -0,62 tot -0,09) en als kans op klinisch relevante respons een OR van 1,9 (95% BI: 1,2 tot 3,1) en een risicoverschil van 13% (95% BI: -4% tot 30%; NNT= 8).
Atypische antipsychotica
De resultaten van de RCT’s naar quetiapine en tiapride konden worden gepoold. Er was geen significant effect vergeleken met placebo: SMD -0,15 (95% BI: -0,43 tot 0,13). De kans op een klinisch relevante respons kon alleen voor één RCT naar quetiapine (Zhong, 2007) en de RCT naar tiapride (Allain, 2000) worden berekend. Dit gaf een gepoolde OR van 1,8 (95% BI: 1,2 tot 2,6) en een risicoverschil van 14% (95% BI: 5% tot 23%; NNT=7).
Voor de individuele RCT’s was de OR 1,76 (95% BI: 1,06 tot 2,94) voor het behandeleffect van quetiapine en 1,86 (95% BI: 1,06 tot 3,24) voor het behandeleffect van tiapride. De SMD voor deze individuele RCT’s bedraagt -0,06 (95% BI: -0,30 tot 0,18) voor quetiapine en -0,39 (95% BI: -0,67 tot -0,11) voor tiapride.
De RCT over risperidon voor agressie leverde een SMD op van -0.38 (95% BI: -0,60 tot -0.15). Het percentage patiënten met een klinische respons werd niet gerapporteerd. Evenmin werd het effect op agitatie gerapporteeerd.
Antidepressiva
Data uit de RCT’s met citalopram en trazodon werd gebruikt voor meta-analyses. Deze gaven een SMD van 0,04 (95% BI: -0,37 tot 0,46) en een kans op een klinisch relevante respons op de CGIC een OR van 1,9 (95% BI: 1,2 tot 3,2) met risicoverschil van 16% (95% BI: 4% tot 28%; NNT=6).
In de RCT naar effect van trazodon (Teri, 2000) is er geen significant effect (gebaseerd op CMAI) als naar de SMD gekeken wordt (SMD= 0,30; 95% BI: -0,17 tot 0,76) en geen significant effect op klinisch relevante respons (OR 1.55 (95% BI: 0,59 tot 4,07).
In de RCT naar effect van citalopram (Porsteinsson, 2014) ontbreekt een significant effect (gebaseerd op CMAI) bij de SMD (SMD= -0,14; 95% BI: -0,44 tot 0,17) en is er wel sprake van een positieve klinische respons (OR= 2,10; 95% BI: 1,17 tot 3,77).
Anti-epileptica
Effectiviteitsdata konden voor vier van de vijf RCT’s (niet uit Olin, 2001) worden gepoold. Dit gaf een SMD van -0,39 (95% BI: -0,83 tot 0,04). Voor een analyse van klinisch relevant respons waren data uit alle RCT’s beschikbaar. Dit gaf een OR van 1,7 (95% BI: 0,7 tot 3,9) en een risicoverschil van 14% (95% BI: -8% tot 36%).
Antidementiemiddelen
Het was mogelijk uit drie RCT’s (m.u.v. Herrmann 2013 en Burns 2011) effectiviteitsdata te extraheren voor een meta-analyse. Deze gaf een SMD van 0,01 (95% BI: -0,18 tot 0,20). Herrmann (2013) rapporteerde ook geen statistisch significante verschillen tussen de interventie- en controlegroep, wat in lijn is met deze gepoolde resultaten. Data uit twee RCT’s (Howard, 2007; Fox, 2012) leidden tot een niet significante kans op een klinisch relevante respons: OR 1,2 (95% BI: 0,7 tot 2,1) met een risicoverschil van 2% (95% BI: -5% tot 8%).
Resultaten en bewijskracht over bijwerkingen van medicatie
Klassieke antipsychotica
Enkel in een haloperidol RCT (Allain, 2000) werd het niet-significant risico op één of meer bijwerkingen gerapporteerd: OR 1,6 (95% BI: 0,9 tot 2,9) en een risicoverschil van 9% (95% BI: -3% tot 22%). Somnolentie was in twee RCT’s beschreven, waaruit het risico kon worden berekend: OR 1,6 (95% BI: 0,8 tot 3,5) en een risicoverschil van 6% (95% BI: -8% tot 20%).
Atypische antipsychotica
In de RCT’s naar quetiapine (Zhong, 2007), tiapride (Allain, 2000) en risperidon (Brodaty, 2003) werden data gerapporteerd over het aantal patiënten met minimaal één bijwerking. Hieruit konden de OR van 1,0 (95% BI: 0,7 tot 1,5) en het risicoverschil van 0% (-5% tot 5%) worden berekend. Daarnaast werden in deze RCT’s het aantal patiënten met somnolentie gegeven, waaruit het niet-significant verhoogd risico op somnolentie kon worden afgeleid: OR 1,7 (95% BI: 1,0 tot 2,9) en risicoverschil van 6% (95% BI: 0% tot 11%)..
Antidepressiva
Enkel de citalopram RCT gaf het aantal patiënten met minimaal één bijwerking. Dit gaf een OR van 1,6 (95% BI: 0,4 tot 5,8) en een risicoverschil van 2% (95% BI: -4% tot 9%), beiden niet significant verhoogd. Specifieke veelvoorkomende bijwerkingen waren in de citalopram RCT significant vaker diarree (OR=2,42; 95% BI: 1,13 tot 5,16; risicoverschil=14%; 95% BI: 2% tot 25%; NNH=7) en in de trazodon RCT niet-significant vaker slaperigheid (OR=1,2; 95% BI: 0,33 tot 4,35; risicoverschil 2%; 95% BI -14% tot 19%).
Anti-epileptica
Alle vijf RCT’s gaven data over het aantal patiënten met één of meer bijwerkingen. Berekening van de OR kwam uit op 2,1 (95% BI: 1,0 tot 4,4) en een risicoverschil van 17% (95% BI: -1% tot 35%). In drie RCT’s (Tariot, 1998; Sommer, 2009 & Porsteinsson, 2001) werd het aantal patiënten met sedatie beschreven, waaruit de kans hierop kon worden bepaald. Dit gaf een OR van 4,0 (95% BI: 0,6 tot 28,9) en een risicoverschil van 19% (95% BI: 2% tot 26%; NNH=5).
Antidementiemiddelen
Geen van de RCT’s beschreef data over patiënten met minimaal één bijwerking. Overigens beschreven Herrmann (2013) en Fox (2012) wel het aantal patiënten met somnolentie, waardoor deze konden worden gepoold: OR=2,2 (95% BI: 1,3 tot 3,9) en risicoverschil 10% (-12% tot 33%). Andere bijwerkingen die opvielen waren agitatie, gestoorde gang, vallen, misselijkheid, duizeligheid en gewichtsafname.
Resultaten en bewijskracht over uitval
Klassieke antipsychotica
Het gepoolde risico op uitval in de drie RCT’s naar haloperidol was niet verhoogd: OR=1,5 (95% BI: 0,9 tot 2,7) en risicoverschil 7% (95% BI: -3% tot 17%).
Atypische antipsychotica
Het gepoolde risico op uitval in de vier RCT’s laat met een 1,1 (95% BI: 0,7% tot 1,9%) en een risicoverschil van 4% (95% BI: -6% tot 14%) geen verschil zien tussen atypische antipsychotica en placebo.
Antidepressiva
Uitval was in alle drie de RCT’s beschreven. Deze gaf in de meta-analyse een niet verhoogd risico op uitval met een OR van 0,9 (95% BI: 0,5 tot 1,8) en risicoverschil -1% (95% BI: -9% tot 7%).
Anti-epileptica
De RCT’s naar vijf anti-epileptica gaven een gepoold niet verhoogd risico op uitval van OR 1,2 (95% BI 0,4 tot 3,5) en risicoverschil 3% (95% BI: -9% tot 16%).
Antidementiemiddelen
Ook in de vijf RCT’s met antidementiemiddelen vertoonden de interventie en controlegroepen geen verschil in uitval: OR 1,1 (95% BI: 0,6 tot 1,9) en risicoverschil 4% (95% BI: -6% tot 14%).
Tabel 6. Evidenceprofiel over psychofarmaca voor geagiteerd gedrag bij mensen met dementie
|
Medicatiegroep uitkomst |
N trials |
Kwaliteit van het bewijs |
n1/ N per groep |
Behandeleffecten |
Algemene beoordeling |
||||||||||
|
Vertekend2 |
inconsistent |
indirect |
Niet precies3 |
Publicatie bias |
medicatie |
placebo |
SMD3 [95% BI] |
OR [95% BI] |
ARR4 [95% BI] |
||||||
|
Klassieke antipsychotica |
|||||||||||||||
|
symptomen |
2 |
ja |
nee |
nee |
ja |
nee |
110/135 |
112/139 |
-0,36 [-0.62; -0.09] |
|
|
laag |
|||
|
Klin. rel. respons |
2 |
ja |
nee |
nee |
nee |
nee |
79/135 |
60/139 |
|
1,9 [1,2; 3,1] |
13% [-4%; 30%]* |
matig |
|||
|
≥1 bijwerkingen |
1 |
ja |
n.v.t. |
nee |
ja |
ja |
77/101 |
69/103 |
|
1,58 [ 0,85; 2,93] |
9% [-3%; 22%] |
laag¥ |
|||
|
uitval |
3 |
nee |
nee |
nee |
ja |
nee |
37/141 |
28/145 |
|
1,52 [0,86; 2,67] |
7% [-3%; 17%] |
matig |
|||
|
Atypische antipsychotica |
|||||||||||||||
|
Symptomen (agitatie) |
3 |
ja |
nee |
nee |
nee |
nee |
363/374 |
222/226 |
-0.15 [-0.43; 0.13]* |
|
|
matig |
|||
|
Symptomen (agressie) |
1 |
ja |
n.v.t. |
nee |
ja |
nee |
149/167 |
152/170 |
-0.38 [-0.60; -0.15]* |
|
|
laag |
|||
|
Klin. rel. Respons (agitatie) |
2 |
ja |
nee |
nee |
nee |
ja5 |
169/343 |
77/195 |
|
1,8 [1,2; 2,6] |
14% [5%; 23% |
laag |
|||
|
≥1 bijwerkingen |
3 |
ja |
nee |
nee |
ja |
ja5 |
419/510 |
300/365 |
|
1,0 [0,7; 1,5] |
0% [-5%; 5%] |
laag¥ |
|||
|
uitval |
4 |
ja |
nee |
nee |
ja |
nee |
162/541 |
100/396 |
|
1,1 [0,7; 1,9]* |
4% [-6%; 14%]* |
laag |
|||
|
Antidepressiva |
|||||||||||||||
|
symptomen |
2 |
ja |
nee |
nee |
nee |
ja |
123/131 |
119/128 |
0,04* [-0,37; 0,46] |
|
|
laag |
|||
|
Klin. rel. respons |
2 |
ja |
nee |
nee |
nee |
ja |
74/131 |
52/128 |
|
1,93 [1,17; 3,19] |
16% [4%; 28%] |
laag |
|||
|
≥1 bijwerkingen |
1 |
ja |
n.v.t. |
nee |
ja |
ja |
90/94 |
86/92 |
|
1,57 [0,43; 5,76] |
2% [-4%; 9%] |
laag¥ |
|||
|
uitval |
3 |
nee |
nee |
nee |
ja |
nee |
20/137 |
21/134 |
|
0,91 [0,46; 1,81] |
-1% [-9%; 7%] |
matig |
|||
|
Anti-epileptica |
|||||||||||||||
|
symptomen |
4 |
ja |
nee |
nee |
ja |
ja |
178/182 |
178/181 |
-0,39 [-0,83; 0,04] |
|
|
erg laag |
|||
|
Klin. rel. respons |
5 |
ja |
ja |
nee |
ja |
nee |
94/191 |
79/193 |
|
1,7 [0,7; 3,9] |
14% [-8%; 36%] |
erg laag |
|||
|
≥1 bijwerkingen |
5 |
ja |
ja |
nee |
ja |
nee |
130/191 |
101/193 |
|
2,1 [1,0; 4,4] |
17% [-1%; 35% |
erg laag |
|||
|
uitval |
5 |
nee |
nee |
nee |
ja |
nee |
33/191 |
27/193 |
|
1,2 [0,4; 3,5] |
3% [-9%; 16%] |
matig |
|||
|
Antidementiemiddelen |
|||||||||||||||
|
symptomen |
3 |
ja |
nee |
nee |
nee |
nee |
209/233 |
214/241 |
0,01 [-0,18; 0,20] |
|
|
matig |
|||
|
Klin. rel. respons |
2 |
ja |
nee |
nee |
ja |
ja |
29/202 |
26/210 |
|
1,18 [0,67; 2,09] |
2% [-5%; 8%] |
laag¥ |
|||
|
≥1 bijwerkingen |
0 |
ja |
n.v.t. |
nee |
ja |
ja |
|
|
|
|
|
erg laag¥ |
|||
|
uitval |
5 |
nee |
ja |
nee |
nee |
nee |
90/452 |
87/467 |
|
1,09* [0,64; 1,88] |
4%* [-6%; 14%] |
matig |
|||
Afkortingen: klin. rel. respons = klinisch relevante respons; SMD = standardized mean difference), OR = odds ratio, ARR = Absolute Risico Reductie, BI = betrouwbaarheidsinterval, NG = niet gerapporteerd.
* op basis van een random model
¥ Niet erg laag, want niet precies hangt samen met publicatiebias
1 n= aantal participanten waarvan data beschikbaar waren voor de uitkomst symptoomreductie, dan wel het aantal participanten met een klinische relevante respons, met >= 1 bijwerkingen, of die uitvielen;
2 = hoge risk of bias;
3 = grote onzekerheid rondom geschatte effect (= BI te breed) door te kleine trials; 3 indien SMD >0.500 dan is sprake van een klinisch relevant effect ;
4 NNT = 100/ ARR voor respons, en NNH= 100/ ARR voor >= 1 bijwerkingen
5 omdat 1 trial deze respons niet vermeldde
Referenties
Allain, H., Dautzenberg, P., Maurer, K., Schuck, S., Bonhomme, D., & Gerard, D. (2000). Double blind study of tiapride versus haloperidol and placebo in agitation and aggressiveness in elderly patients with cognitive impairment. Psychopharmacology, (148), 361–366.
Ancoli-Israel, S., Gehrman, P., Martin, J. L., Shochat, T., Marler, M., Corey-Bloom, J., & Levi, L. (2003). Increased light exposure consolidates sleep and strengthens circadian rhythms in severe Alzheimer’s disease patients. Behavioral Sleep Medicine, 1(1), 22–36.
Ancoli-Israel, S., Martin, J. L., Gehrman, P., Shochat, T., Corey-Bloom, J., Marler, M., … Levi, L. (2003). Effect of light on agitation in institutionalized patients with severe Alzheimer disease. The American Journal of Geriatric Psychiatry : Official Journal of the American Association for Geriatric Psychiatry, 11(2), 194–203.
Auchus, A., & Bissey-Black, C. (1997). Pilot Study of Haloperidol, and Placebo Agitation in Alzheimer’s Disease. Neuropsychiatry and Clinical Neurosciences, 9, 591–593.
Ayalon, L., Gum, A. M., Feliciano, L., & Areán, P. A. (2006). Effectiveness of nonpharmacological interventions for the management of neuropsychiatric symptoms in patients with dementia: a systematic review. Archives of internal medicine, 166(20), 2182-2188.
Baillon, S., Van Diepen, E., Prettyman, R., Redman, J., Rooke, N., & Campbell, R. (2004). A comparison of the effects of Snoezelen and reminiscence therapy on the agitated behaviour of patients with dementia. International journal of geriatric psychiatry, 19: 1047-1052.
Ballard, C., Brown, R., Fossey, J., Douglas, S., Bradley, P., Hancock, J., ... & Lindesay, J. (2009). Brief psychosocial therapy for the treatment of agitation in Alzheimer disease (the CALM-AD trial). The American journal of geriatric psychiatry, 17(9), 726-733.
Ballard, C., Margallo-Lana, M., Juszczak, E., Douglas, S., Swann, A., Thomas, A., … Jacoby, R. (2005). Quetiapine and rivastigmine and cognitive decline in Alzheimer’s disease: randomised double blind placebo controlled trial. BMJ, 330(7496), 874.
Beck, C. K., Vogelpohl, T. S., Rasin, J. H., Uriri, J. T., O’sullivan, P., Walls, R., ... & Baldwin, B. (2002). Effects of behavioral interventions on disruptive behavior and affect in demented nursing home residents. Nursing research, 51(4), 219-228.
Beller, S. A., & Overall, J. E. (1984). The Brief Psychiatric Rating Scale (BPRS) in geropsychiatric research: II. Representative profile patterns. Journal of Gerontology, 39(2), 194–200.
Brasure, M., Jutkowitz, E., Fuchs, E., Nelson, V. A., Kane, R. A., Shippee, T., ... & Kane, R. L. (2016). Nonpharmacologic Interventions for Agitation and Aggression in Dementia. internet.
Brodaty, H., Ames, D., Snowdon, J., Woodward, M., Kirwan, J., Clarnette, R. Lee, E., Lyons B. and Grossman F. (2003). A randomized placebo-controlled trial of risperidone for the treatment of aggression, agitation, and psychosis of dementia. J Clin Psychiatry 64(2): 134-143.
Buettner, L. L., Lundegren, H., Lago, D., Farrell, P., & Smith, R. (1996). Therapeutic recreation as an intervention for persons with dementia and agitation: An efficacy study. American Journal of Alzheimer's Disease, 11(5), 4-12.
Burns, A., Allen, H., Tomenson, B., Duignan, D., & Byrne, J. (2009). Bright light therapy for agitation in dementia: a randomized controlled trial. International Psychogeriatrics / IPA, 21(4), 711–721.
Burns, A., Perry, E., Holmes, C., Francis, P., Morris, J., Howes, M. J., ... & Ballard, C. (2011). A double-blind placebo-controlled randomized trial of Melissa officinalis oil and donepezil for the treatment of agitation in Alzheimer’s disease. Dementia and geriatric cognitive disorders, 31(2), 158-164.
Burns, A., Perry, E., Holmes, C., Francis, P., Morris, J., Howes, M. J., Ballard, C. (2011). A double-blind placebo-controlled randomized trial of Melissa officinalis oil and donepezil for the treatment of agitation in Alzheimer’s disease. Dement Geriatr Cogn Disord, 31(2), 158–164.
Chenoweth, L., Forbes, I., Fleming, R., King, M. T., Stein-Parbury, J., Luscombe, G., ... & Brodaty, H. (2014). PerCEN: a cluster randomized controlled trial of person-centered residential care and environment for people with dementia. International Psychogeriatrics, 26(7), 1147-1160.
Cohen-Mansfield, J., Marx, M. S., & Rosenthal, A. S. (1989). A description of agitation in a nursing home. Journal of Gerontology, 44(3), M77-84.
Cohen-Mansfield, J., Thein, K., Marx, M. S., Dakheel-Ali, M., & Freedman, L. (2012). Efficacy of nonpharmacologic interventions for agitation in advanced dementia: a randomized, placebo-controlled trial. The Journal of clinical psychiatry, 73(9), 1255-1261.
Cooke, M. L., Moyle, W., Shum, D. H., Harrison, S. D., & Murfield, J. E. (2010). A randomized controlled trial exploring the effect of music on agitated behaviours and anxiety in older people with dementia. Aging and mental health, 14(8), 905-916.
Craig, J. (2014) Music therapy to reduce agitation in dementia. Nursing Times 110 (32-33), 12-15.
Cummings, J. L., Lyketsos, C. G., Peskind, E. R., Porsteinsson, A. P., Mintzer, J. E., Scharre, D. W., … Siffert, J. (2015). Effect of Dextromethorphan-Quinidine on Agitation in Patients With Alzheimer Disease Dementia. Jama, 314(12), 1242.
Forrester, L. T., Maayan, N., Orrell, M., Spector, A. E., Buchan, L. D., & Soares‐Weiser, K. (2014). Aromatherapy for dementia. The Cochrane Library.
Fu, C. Y., Moyle, W., & Cooke, M. (2013). A randomised controlled trial of the use of aromatherapy and hand massage to reduce disruptive behaviour in people with dementia. BMC complementary and alternative medicine, 13(1), 165.
Garland, K., Beer, E., Eppingstall, B., & O'Connor, D. W. (2007). A comparison of two treatments of agitated behavior in nursing home residents with dementia: simulated family presence and preferred music. The American journal of geriatric psychiatry, 15(6), 514-521.
Gerdner, L. A. (2000). Effects of individualized versus classical “relaxation” music on the frequency of agitation in elderly persons with Alzheimer's disease and related disorders. International Psychogeriatrics, 12(01), 49-65.
Gormley, N., Lyons, D., & Howard, R. (2001). Behavioural management of aggression in dementia: a randomized controlled trial. Age and Ageing, 30(2), 141-145.
Groene, R. W. (1993). Effectiveness of music therapy 1: 1 intervention with individuals having senile dementia of the Alzheimer's type. Journal of Music Therapy, 30(3), 138-157.
Guy, W. (Ed.). (1976). ECDEU Assessment Manual for Psychopharmacology. In Publication #ADM 76-338 (pp. 217–222). Rockville, MD: U.S. Dept. of Health, Education, and Welfare.
Hawranik, P., Johnston, P., & Deatrich, J. (2008). Therapeutic touch and agitation in individuals with Alzheimer's disease. Western journal of nursing research, 30(4), 417-434.
Helmes, E. (1988). Multidimensional Observation Scale for Elderly Subjects (MOSES). Psychopharmacology Bulletin, 24(4), 733–745.
Hicks-Moore, S. L., & Robinson, B. A. (2008). Favorite music and hand massage Two interventions to decrease agitation in residents with dementia. Dementia, 7(1), 95-108.
Howard, R. J., Juszczak, E., Ballard, C. G., Bentham, P., Brown, R. G., Bullock, R., … Rodger, M. (2007). Donepezil for the treatment of agitation in Alzheimer’s disease. The New England Journal of Medicine, 357(14), 1382–1392.
Huang, H. L., Kuo, L. M., Chen, Y. S., Liang, J., Huang, H. L., Chiu, Y. C., ... & Shyu, Y. I. L. (2013). A home-based training program improves caregivers' skills and dementia patients' aggressive behaviors: a randomized controlled trial. The American journal of geriatric psychiatry, 21(11), 1060-1070.
Huang, H. L., Shyu, Y. I. L., Chen, M. C., Chen, S. T., & Lin, L. C. (2003). A pilot study on a home‐based caregiver training program for improving caregiver self‐efficacy and decreasing the behavioral problems of elders with dementia in Taiwan. International journal of geriatric psychiatry, 18(4), 337-345.
Iverson, G. L., Hopp, G. A., DeWolfe, K., & Solomons, K. (2002). Measuring change in psychiatric symptoms using the Neuropsychiatric Inventory: Nursing Home version. International Journal of Geriatric Psychiatry, 17(5), 438–443.
Jutkowitz, E., Brasure, M., Fuchs, E., Shippee, T., Kane, R. A., Fink, H. A., ... & Kane, R. L. (2016). Care‐Delivery Interventions to Manage Agitation and Aggression in Dementia Nursing Home and Assisted Living Residents: A Systematic Review and Meta‐analysis. Journal of the American Geriatrics Society, 64(3), 477-488.
Kong, E. H., Evans, L. K., & Guevara, J. P. (2009). Nonpharmacological intervention for agitation in dementia: a systematic review and meta-analysis. Aging & mental health, 13(4), 512-520.
Kovach, C. R., Taneli, Y., Dohearty, P., Schlidt, A. M., Cashin, S., & Silva-Smith, A. L. (2004). Effect of the BACE intervention on agitation of people with dementia. The Gerontologist, 44(6), 797-806.
Lin, L. C., Yang, M. H., Kao, C. C., Wu, S. C., Tang, S. H., & Lin, J. G. (2009). Using acupressure and Montessori‐based activities to decrease agitation for residents with dementia: a cross‐over trial. Journal of the American Geriatrics Society, 57(6), 1022-1029.
Lin, P. W. K., Chan, W. C., Ng, B. F. L., & Lam, L. C. W. (2007). Efficacy of aromatherapy (Lavandula angustifolia) as an intervention for agitated behaviours in Chinese older persons with dementia: a cross‐over randomized trial. International journal of geriatric psychiatry, 22(5), 405-410.
Lindenmayer, J.-P., Brown, E., Baker, R. W., Schuh, L. M., Shao, L., Tohen, M., Stauffer, V. L. (2004). An excitement subscale of the Positive and Negative Syndrome Scale. Schizophrenia Research, 68(2–3), 331–337.
Livingston, G., Kelly, L., Lewis-Holmes, E., Baio, G., Morris, S., Patel, N., ... & Cooper, C. (2014). Non-pharmacological interventions for agitation in dementia: systematic review of randomised controlled trials. The British Journal of Psychiatry, 205(6), 436-442.
Livingston, G., Kelly, L., Lewis-Holmes, E., Baio, G., Morris, S., Patel, N., ... & Cooper, C. (2014). A systematic review of the clinical effectiveness and cost-effectiveness of sensory, psychological and behavioural interventions for managing agitation in older adults with dementia. Health Technology Assessment 18, 1-226.
Lyketsos, C. G., Lindell Veiel, L., Baker, A., & Steele, C. (1999). A randomized, controlled trial of bright light therapy for agitated behaviors in dementia patients residing in long-term care. International Journal of Geriatric Psychiatry, 14(7), 520–525.
McCallion, P., Toseland, R. W., & Freeman, K. (1999). An evaluation of a family visit education program. Journal of the American Geriatrics Society, 47(2), 203-214.
Moyle, W., Cooke, M. L., Beattie, E., Shum, D. H., O’Dwyer, S. T., & Barrett, S. (2014). Foot massage versus quiet presence on agitation and mood in people with dementia: A randomised controlled trial. International journal of nursing RCT’s, 51(6), 856-864
NCT02686190. Effects of Light-therapy in Alzheimer’s Disease (ALZ-Light).
O’Connor, D. W., Eppingstall, B., Taffe, J., & van der Ploeg, E. S. (2013). A randomized, controlled cross-over trial of dermally-applied lavender (Lavandula angustifolia) oil as a treatment of agitated behaviour in dementia. BMC complementary and alternative medicine, 13(1), 315.
Olin, J. T., Fox, L. S., Pawluczyk, S., Taggart, N. A., & Schneider, L. S. (2001). A pilot randomized trial of carbamazepine for behavioral symptoms in treatment-resistant outpatients with Alzheimer disease. Am J Geriatr Psychiatry, 9(4), 400–405.
Oliveira, A. M. D., Radanovic, M., Mello, P. C. H. D., Buchain, P. C., Vizzotto, A. D. B., Celestino, D. L., ... & Forlenza, O. V. (2015). Nonpharmacological Interventions to Reduce Behavioral and Psychological Symptoms of Dementia: A Systematic Review. BioMed research international, 2015.
O'Neil, M. E., Freeman, M., Christensen, V., Telerant, R., Addleman, A., & Kansagara, D. (2011). A systematic evidence review of non-pharmacological interventions for behavioral symptoms of dementia. Washington, DC: Department of Veterans Affairs.
Opie, J., Doyle, C., & O'Connor, D. W. (2002). Challenging behaviours in nursing home residents with dementia: a randomized controlled trial of multidisciplinary interventions. International journal of geriatric psychiatry, 17(1), 6-13.
Porsteinsson, A. P., Drye, L. T., Pollock, B. G., Devanand, D. P., Frangakis, C., Ismail, Z., … Lyketsos, C. G. (2014). Effect of citalopram on agitation in Alzheimer disease: the CitAD randomized clinical trial. Jama, 311(7), 682–91.
Porsteinsson, A. P., Tariot, P. N., Erb, R., Cox, C., Smith, E., Jakimovich, L., … Irvine, C. (2001). Placebo-controlled study of divalproex sodium for agitation in dementia. Am J Geriatr Psychiatry, 9(1), 58–66.
Rabinowitz, J., Davidson, M., De Deyn, P.P., Katz, I., Brodaty, H. & Cohen-Mansfield, J. (2005). Factor analysis of the Cohen-Mansfield Agitation Inventory in three large samples of nursing home patients with dementia and behavioral disturbance. Am J Geriatric Psychiatry, 13, 991-998.
Randall, E. W., & Clissett, P. C. (2016). What are the relative merits of interventions used to reduce the occurrences of disruptive vocalisation in persons with dementia?–a systematic review. International Journal of Older People Nursing, 11(1), 4-17.
Reisberg, B., Borenstein, J., Salob, S. P., Ferris, S. H., Franssen, E., & Georgotas, A. (1987). Behavioral symptoms in Alzheimer’s disease: phenomenology and treatment. The Journal of Clinical Psychiatry, 48 Suppl, 9–15.
Remington, R. (2002). Calming music and hand massage with agitated elderly. Nursing research, 51(5), 317-323.
Reuther, S., Dichter, M. N., Buscher, I., Vollmar, H. C., Holle, D., Bartholomeyczik, S., & Halek, M. (2012). Case conferences as interventions dealing with the challenging behavior of people with dementia in nursing homes: a systematic review. International Psychogeriatrics, 24(12), 1891-1903.
Ridder, H. M. O., Stige, B., Qvale, L. G., & Gold, C. (2013). Individual music therapy for agitation in dementia: an exploratory randomized controlled trial. Aging & mental health, 17(6), 667-678.
Rosen, J., Burgio, L., Kollar, M., Cain, M., Allison, M., Fogleman, M., … Zubenko, G. S. (1994). A user-friendly instrument for rating agitation in dementia patients. The American Journal of Geriatric Psychiatry : Official Journal of the American Association for Geriatric Psychiatry, 2(1), 52–59.
Sloane, P. D., Hoeffer, B., Mitchell, C. M., McKenzie, D. A., Barrick, A. L., Rader, J., ... & Koch, G. G. (2004). Effect of person‐centered showering and the towel bath on bathing‐associated aggression, agitation, and discomfort in nursing home residents with dementia: A randomized, controlled trial. Journal of the American Geriatrics Society, 52(11), 1795-1804.
Snyder M, Egan EC, Burns KR. Interventions for decreasing agitation behaviors in persons with dementia. J Gerontol Nurs. 1995 Jul;21(7):34-40.
Sommer, O. H., Aga, O., Cvancarova, M., Olsen, I. C., Selbaek, G., & Engedal, K. (2009). Effect of oxcarbazepine in the treatment of agitation and aggression in severe dementia. Dement Geriatr Cogn Disord, 27(2), 155–163.
Sung, H. C., Chang, S. M., Lee, W. L., & Lee, M. S. (2006). The effects of group music with movement intervention on agitated behaviours of institutionalized elders with dementia in Taiwan. Complementary therapies in medicine, 14(2), 113-119.
Tariot, P. N., Erb, R., Podgorski, C. A., Cox, C., Patel, S., Jakimovich, L., & Irvine, C. (1998). Efficacy and tolerability of carbamazepine for agitation and aggression in dementia. Am J Psychiatry, 155(1), 54–61.
Teri, L., Logsdon, R. G., & Peskind, E. (2000). Treatment of agitation in AD: A randomized, placebo-controlled clinical trial. Neurology, 55(November), 1271–1277.
Testad, I., Corbett, A., Aarsland, D., Lexow, K. O., Fossey, J., Woods, B., & Ballard, C. (2014). The value of personalized psychosocial interventions to address behavioral and psychological symptoms in people with dementia living in care home settings: a systematic review. International psychogeriatrics, 26(07), 1083-109.
van der Ploeg, E. S., Eppingstall, B., Camp, C. J., Runci, S. J., Taffe, J., & O'Connor, D. W. (2013). A randomized crossover trial to study the effect of personalized, one-to-one interaction using Montessori-based activities on agitation, affect, and engagement in nursing home residents with Dementia. International psychogeriatrics, 25(04), 565-575.
Vink, A. C., Zuidersma, M., Boersma, F., Jonge, P., Zuidema, S. U., & Slaets, J. P. J. (2013). The effect of music therapy compared with general recreational activities in reducing agitation in people with dementia: a randomised controlled trial. International journal of geriatric psychiatry, 28(10), 1031-1038.
Visser, S. M., McCabe, M. P., Hudgson, C., Buchanan, G., Davison, T. E., & George, K. (2008). Managing behavioural symptoms of dementia: effectiveness of staff education and peer support. Aging and Mental Health, 12(1), 47-55.
Wright, L. K., Litaker, M., Laraia, M. T., & DeAndrade, S. (2001). Continuum of care for Alzheimer's disease: a nurse education and counseling program. Issues in mental health nursing, 22(3), 231-252.
Yang, M. H., Lin, L. C., Wu, S. C., Chiu, J. H., Wang, P. N., & Lin, J. G. (2015). Comparison of the efficacy of aroma-acupressure and aromatherapy for the treatment of dementia-associated agitation. BMC complementary and alternative medicine, 15(1), 93.
Zhong, K., Tariot, P., Mintzer, J., Minkwitz, M., & Devine, N. (2007). Quetiapine to Treat Agitation in Dementia : A Randomized , Double-Blind , Placebo-Controlled Study. Current Alzheimer Research, 4(1), 81–93.
Zuidema SU, Derksen E, Verhey FRJ, Koopmans RTCM. Prevalence of neuropsychiatric symptoms in a large sample of Dutch nursing home patients with dementia. Int J Geriatr Psychiatry 2007; 22: 632-638.
Bijlagen psychosociale en psychologische interventies
Bijlage 1.1. Exclusietabel van RCT’s naar psychosociale en psychologische interventies voor geagiteerd gedrag bij mensen met dementie (exclusie na lezen van volledige artikel).
|
Referentie |
Reden van exclusie |
|
Primaire RCT’s (RCT’s) voor agitatie |
|
|
Ballard, C., Brown, R., Fossey, J., Douglas, S., Bradley, P., Hancock, J., ... & Lindesay, J. (2009). Brief psychosocial therapy for the treatment of agitation in Alzheimer disease (the CALM-AD trial). The American journal of geriatric psychiatry, 17(9), 726-733. |
Design: geen RCT |
|
Haupt, M., Karger, A., & Jänner, M. (2000). Improvement of agitation and anxiety in demented patients after psychoeducative group intervention with their caregivers. International journal of geriatric psychiatry, 15(12), 1125-1129. |
Geen specifieke indicatie agitatie |
|
Jøranson, N., Pedersen, I., Rokstad, A. M. M., & Ihlebæk, C. (2015). Effects on Symptoms of Agitation and Depression in Persons With Dementia Participating in Robot-Assisted Activity: A Cluster-Randomized Controlled Trial. Journal of the American Medical Directors Association, 16(10), 867-873. |
Geen specifieke indicatie agitatie |
|
Olsen, C., Pedersen, I., Bergland, A., Enders‐Slegers, M. J., Patil, G., & Ihlebæk, C. (2016). Effect of animal‐assisted interventions on depression, agitation and quality of life in nursing home residents suffering from cognitive impairment or dementia: a cluster randomized controlled trial. International journal of geriatric psychiatry, 1-10. |
Geen specifieke indicatie agitatie |
|
Sánchez, A., Maseda, A., Marante-Moar, M. P., de Labra, C., Lorenzo-López, L., & Millán-Calenti, J. (2016). Comparing the effects of multisensory stimulation and individualized music sessions on elderly people with severe dementia: a randomized controlled trial. Journal of Alzheimer's Disease, (Preprint), 1-13. |
Geen specifieke indicatie agitatie |
|
Staal, J. A., Amanda, S., Matheis, R., Collier, L., Calia, T., Hanif, H., & Kofman, E. S. (2007). The effects of Snoezelen (multi-sensory behavior therapy) and psychiatric care on agitation, apathy, and activities of daily living in dementia patients on a short term geriatric psychiatric inpatient unit. The International Journal of Psychiatry in Medicine, 37(4), 357-370. |
Geen specifieke indicatie agitatie |
|
Testad, I., Ballard, C., Brønnick, K., & Aarsland, D. (2010). The effect of staff training on agitation and use of restraint in nursing home residents with dementia: a single-blind, randomized controlled trial. The Journal of clinical psychiatry, 71(1), 80-86. |
Geen specifieke indicatie agitatie |
|
Woods DL, Beck C, Sinha K. The effect of therapeutic touch on behavioral |
geen RCT |
|
Systematische reviews voor agitatie |
|
|
Ayalon, L., Gum, A. M., Feliciano, L., & Areán, P. A. (2006). Effectiveness of nonpharmacological interventions for the management of neuropsychiatric symptoms in patients with dementia: a systematic review. Archives of internal medicine, 166(20), 2182-2188. Behalve McCallion, 1999, zijn alle overige RCT’s geëxcludeerd. |
Geen specifieke indicatie agitatie |
|
Moniz Cook, E. D., Swift, K., James, I., Malouf, R., De Vugt, M., & Verhey, F. (2012). Functional analysis‐based interventions for challenging behaviour in dementia. The Cochrane Library. |
Geen specifieke indicatie agitatie |
|
Oliveira, A. M. D., Radanovic, M., Mello, P. C. H. D., Buchain, P. C., Vizzotto, A. D. B., Celestino, D. L., ... & Forlenza, O. V. (2015). Nonpharmacological Interventions to Reduce Behavioral and Psychological Symptoms of Dementia: A Systematic Review. BioMed research international, 2015.
Behalve Garland 2007 en Gerdner 2000 (muziek) zijn de overige RCT’s geëxcludeerd. |
Geen specifieke indicatie agitatie |
|
O'Neil, M. E., Freeman, M., Christensen, V., Telerant, R., Addleman, A., & Kansagara, D. (2011). A systematic evidence review of non-pharmacological interventions for behavioral symptoms of dementia. Washington, DC: Department of Veterans Affairs. Behalve McCallion, 1999, Gerdner, 2000, Groene 1993 en Beck 2002 zijn alle overige RCT’s geëxcludeerd. |
Geen specifieke indicatie agitatie |
|
Padilla, R. (2011). Effectiveness of environment-based interventions for people with Alzheimer’s disease and related dementias. American Journal of Occupational Therapy, 65(5), 514-522. |
Geen specifieke indicatie agitatie |
|
Spira, A. P., & Edelstein, B. A. (2006). Behavioral interventions for agitation in older adults with dementia: an evaluative review. International Psychogeriatrics, 18(02), 195-225. |
Design: geen systematic review |
|
Staedtler, A. V., & Nunez, D. (2015). Nonpharmacological Therapy for the Management of Neuropsychiatric Symptoms of Alzheimer's Disease: Linking Evidence to Practice. Worldviews on Evidence‐Based Nursing, 12(2), 108-115. |
Geen specifieke indicatie agitatie |
|
Teri, L., Logsdon, R. G., & McCurry, S. M. (2002). Nonpharmacologic treatment of behavioral disturbance in dementia. Medical Clinics of North America, 86(3), 641-656. |
Design: geen systematic review |
|
Thuné-Boyle, I. C. V., Iliffe, S., Cerga-Pashoja, A., Lowery, D., & Warner, J. (2012). The effect of exercise on behavioral and psychological symptoms of dementia: towards a research agenda. International Psychogeriatrics, 24(07), 1046-1057. |
Geen specifieke indicatie agitatie |
|
Liu, W., Cheon, J., & Thomas, S. A. (2014). Interventions on mealtime difficulties in older adults with dementia: a systematic review. International journal of nursing RCT’s, 51(1), 14-27. |
Agitatie geen primaire uitkomstmaat |
|
Whear, R., Abbott, R., Thompson-Coon, J., Bethel, A., Rogers, M., Hemsley, A., ... & Stein, K. (2014). Effectiveness of mealtime interventions on behavior symptoms of people with dementia living in care homes: a systematic review. Journal of the American Medical Directors Association, 15(3), 185-193. |
De geïncludeerde RCT’s zijn geen RCT’s |
|
Whear, R., Coon, J. T., Bethel, A., Abbott, R., Stein, K., & Garside, R. (2014). What is the impact of using outdoor spaces such as gardens on the physical and mental well-being of those with dementia? A systematic review of quantitative and qualitative evidence. Journal of the American Medical Directors Association, 15(10), 697-705. |
De geïncludeerde RCT’s zijn geen RCT’s |
Bijlage 1.2. Risico op bias psychosociale en psychologische interventies voor geagiteerd gedrag bij mensen met dementie
|
|
1. randomisatie proces |
2. afwijkingen van beoogde interventie |
3. ontbrekende uitkomsten |
4. uitkomstmetingen |
5. selectieve rapportage |
6. overig |
totaal aantal items zonder bias |
|
|
Activiteitentherapie |
||||||||
|
Van der Ploeg, 2013 |
Geen |
Wel |
Wel |
Onduidelijk |
geen |
Geen |
3/6 |
|
|
Lin, 2009 |
Onduidelijk |
Wel |
Geen |
Geen |
Geen |
Geen |
4/6 |
|
|
Kovach, 2004 |
Onduidelijk |
Wel |
Wel |
Geen |
Geen |
Geen |
3/6 |
|
|
Beuttner, 1996 |
Onduidelijk |
Wel |
Wel |
Wel |
Geen |
Geen |
2/6 |
|
|
Muziekinterventies |
||||||||
|
Cooke 2010 |
Wel bias |
Wel bias |
Geen bias |
Geen bias |
Wel bias |
Geen bias |
3/6 |
|
|
Gerdner 2000 |
Wel bias |
Wel bias |
Wel bias |
Wel bias |
Wel bias |
Geen bias |
1/6 |
|
|
Garland 2007 |
Wel bias |
Wel bias |
Geen bias |
Wel bias |
Wel bias |
Geen bias |
2/6 |
|
|
Vink 2012 |
Wel bias |
Wel bias |
Wel bias |
Wel bias |
Geen bias |
Geen bias |
2/6 |
|
|
Groene 1993 |
Wel bias |
Wel bias |
Geen bias |
Wel bias |
Wel bias |
Wel bias |
1/6 |
|
|
Ridder 2013 |
Geen bias |
Wel bias |
Wel bias |
Wel bias |
Geen bias |
Geen bias |
3/6 |
|
|
Hicks-Moore 2008 |
Wel bias |
Wel bias |
Geen bias |
Wel bias |
Wel bias |
Wel bias |
1/6 |
|
|
Remington |
Geen bias |
Wel bias |
Geen bias |
Wel bias |
Wel bias |
Geen bias |
3/6 |
|
|
Zintuiglijke interventies |
||||||||
|
Baillon 2004 |
Wel bias |
Wel bias |
Wel bias |
Wel bias |
Wel bias |
Wel bias |
0/6 |
|
|
Hawrink |
Wel bias |
Wel bias |
Wel bias |
Geen bias |
Wel bias |
Geen bias |
2/6 |
|
|
Lin 2009 |
Wel bias |
Wel bias |
Geen bias |
Wel bias |
Geen bias |
Geen bias |
3/6 |
|
|
Moyle 2014 |
Geen bias |
Wel bias |
Geen bias |
Geen bias |
Wel bias |
Wel bias |
3/6 |
|
|
Hicks-Moore 2008 |
Wel bias |
Wel bias |
Geen bias |
Wel bias |
Wel bias |
Wel bias |
1/6 |
|
|
Remington |
Geen bias |
Wel bias |
Geen bias |
Wel bias |
Wel bias |
Geen bias |
3/6 |
|
|
Fu, 2013 |
Geen |
Wel |
Onduidelijk |
Onduidelijk |
Wel |
Geen |
2/6 |
|
|
Aromatherapie |
||||||||
|
Lin, 2007 |
Onduidelijk |
Onduidelijk |
Geen |
Onduidelijk |
Geen |
Geen |
3/6 |
|
|
O’Connor, 2013 |
Onduidelijk |
Onduidelijk |
Wel |
Geen |
Geen |
Geen |
3/6 |
|
|
Yang, 2015 |
Onduidelijk |
Onduidelijk |
Wel |
Geen |
Geen |
Geen |
3/6 |
|
|
Burns, 2011 |
Wel bias |
Onduidelijk |
Geen bias |
Geen bias |
Geen bias |
Wel bias |
3/6 |
|
|
Ballard 2002 |
Geen |
Onduidelijk |
Wel |
Geen |
Geen |
Geen |
4/6 |
|
|
Fu, 2013 |
Geen |
Wel |
Onduidelijk |
Onduidelijk |
Wel |
Geen |
2/6 |
|
|
Mediatieve interventies |
||||||||
|
Gormley, 2001 |
Wel |
Wel |
Wel |
Geen |
Geen |
Geen |
3/6 |
|
|
Huang, 2003 |
Wel |
Geen |
Wel |
Onduidelijk |
Geen |
Geen |
3/6 |
|
|
Huang, 2013 |
Wel |
Wel |
Geen |
Wel |
Wel |
Geen |
2/6 |
|
|
Wright, 2001 |
Onduidelijk |
Wel |
Geen |
Wel |
Geen |
Geen |
3/6 |
|
|
Chenoweth, 2014 |
Geen |
Wel |
Wel |
Geen |
Geen |
Geen |
4/6 |
|
|
McCallion, 1999 |
Wel |
Wel |
Geen |
Geen |
Geen |
Geen |
4/6 |
|
|
Sloane, 2004 |
Onduidelijk |
Wel |
Wel |
Geen |
Geen |
Geen |
3/6 |
|
|
Visser, 2008 |
Wel |
Wel |
Onduidelijk |
Wel |
Geen |
Geen |
2/6 |
|
|
Beck 2002 |
Wel bias |
Wel bias |
Wel bias |
Wel bias |
Geen bias |
Geen bias |
2/6 |
|
|
Overige interventies |
||||||||
|
Garland 2007 |
Wel bias |
Wel bias |
Geen bias |
Wel bias |
Wel bias |
Geen bias |
2/6 |
|
|
Opie |
Wel bias |
Wel bias |
Geen bias |
Wel bias |
Geen bias |
Wel bias |
2/6 |
|
|
Sung 2006 |
Geen bias |
Wel bias |
Wel bias |
Wel bias |
Geen bias |
Geen bias |
3/6 |
|
|
Cohen-Mansfield 2012 |
Wel bias |
Wel bias |
Welk bias |
Geen bias |
Geen bias |
Geen bias |
3/6 |
|
Bijlagen inzet lichttherapie
Bijlage 2.1. Exclusietabel van RCT’s naar lichttherapie voor geagiteerd gedrag bij mensen met dementie
|
Referentie |
Reden van exclusie |
|
Primaire RCT’s |
|
|
Figueiro, M. G., Plitnick, B. A., Lok, A., Jones, G. E., Higgins, P., Hornick, T. R., & Rea, M. S. (2014). Tailored lighting intervention improves measures of sleep, depression, and agitation in persons with Alzheimer’s disease and related dementia living in long-term care facilities. Clinical Interventions in Aging, 9, 1527–1537. |
Trial, geen parallelle groepen. |
|
Mishima, K., Hishikawa, Y., & Okawa, M. (1998). Randomized, dim light controlled, crossover test of morning bright light therapy for rest-activity rhythm disorders in patients with vascular dementia and dementia of Alzheimer’s type. Chronobiology International, 15(6), 647–654. |
Trial, geen parallelle groepen. |
|
Riemersma-van der Lek, R. F., Swaab, D. F., Twisk, J., Hol, E. M., Hoogendijk, W. J., & Van Someren, E. J. (2008). Effect of Bright Light and Melatonin on Cognitive and Noncognitive Function in Elderly Residents of Group Care Facilities. Jama, 299(22), 2642. |
Trial, geen specifieke indicatie agressief gedrag |
|
Dowling, G. A., Graf, C. L., Hubbard, E. M., & Luxenberg, J. S. (2007). Light treatment for neuropsychiatric behaviors in Alzheimer’s disease. Western Journal of Nursing Research, 29(8), 961–975. |
Trial, geen specifieke indicatie agressief gedrag |
|
Fontana Gasio, P., Kräuchi, K., Cajochen, C., Van Someren, E., Amrhein, I., Pache, M., Wirz-Justice, A. (2003). Dawn-dusk simulation light therapy of disturbed circadian rest-activity cycles in demented elderly. Exp Gerontol, 38(1–2), 207–216. |
Trial, geen specifieke indicatie agressief gedrag |
|
Haffmans, P. M., Sival, R. C., Lucius, S. A., Cats, Q., & van Gelder, L. (2001). Bright light therapy and melatonin in motor restless behaviour in dementia: a placebo-controlled study. Int J Geriatr Psychiatry, 16(1), 106–110. Journal Article. |
Trial van licht met melatonine versus licht met placebo. |
|
Systematische reviews |
|
|
Forbes, D., Blake, C. M., Thiessen, E. J., Peacock, S., & Hawranik, P. (2014). Light therapy for improving cognition, activities of daily living, sleep, challenging behaviour, and psychiatric disturbances in dementia. Cochrane Database Syst Rev, 2, Cd003946. |
Meta-analyse waarvan niet alle RCT’s voldoen aan onze inclusiecriteria. |
Bijlage 2.2 Risico op bias van RCT’s naar lichttherapie voor geagiteerd gedrag bij mensen met dementie
|
|
1. randomisatieproces |
2. afwijkingen van beoogde interventie |
3. ontbrekende uitkomsten |
4. uitkomst-metingen |
5. selectieve rapportage |
6. overig |
aantal items zonder bias |
|
Burns 2009 |
onduidelijk |
geen bias |
geen bias |
geen bias |
wel bias |
onduidelijk |
3 |
|
Ancoli-Israel 2003a/b |
onduidelijk |
onduidelijk |
onduidelijk |
geen bias |
onduidelijk |
geen bias |
2 |
|
Lyketsos 1999 |
onduidelijk |
onduidelijk |
wel bias |
geen bias |
geen bias |
wel bias |
2 |
Bijlagen inzet psychofarmaca
Bijlage 3.1 Exclusietabel psychofarmaca voor geagiteerd gedrag bij mensen met dementie (na lezen van volledig artikel)
|
Referentie |
Reden van exclusie |
|
Primaire RCT’s |
|
|
Asayama, K., Yamadera, H., Ito, T., Suzuki, H., Kudo, Y., & Endo, S. (2003). Double blind study of melatonin effects on the sleep-wake rhythm, cognitive and non-cognitive functions in Alzheimer type dementia. J Nippon Med Sch, 70(4), 334–341. |
Trial, geen specifieke indicatie agressief gedrag |
|
Ballard, C., Thomas, A., Gerry, S., Yu, L. M., Aarsland, D., Merritt, C., … Walker, Z. (2015). A double-blind randomized placebo-controlled withdrawal trial comparing memantine and antipsychotics for the long-term treatment of function and neuropsychiatric symptoms in people with Alzheimer’s disease (MAIN-AD). J Am Med Dir Assoc, 16(4), 316–322. |
Trial, niet placebo-gecontroleerd |
|
Barnes, R., Veith, R., Okimoto, J., Raskind, M., & Gumbrecht, G. (1982). Efficacy of Antipsychotic Medications in Behaviorally Disturbed Dementia Patients. Am J Psychiatry, 139(9), 1170–1174. |
Trial, geen specifieke indicatie agressief gedrag |
|
Brodaty, H., Ames, D., Snowdon, J., Woodward, M., Kirwan, J., Clarnette, R., … Greenspan, A. (2005). Risperidone for psychosis of Alzheimer’s disease and mixed dementia: results of a double-blind, placebo-controlled trial. Int J Geriatr Psychiatry, 20(12), 1153–7. |
Trial, geen specifieke indicatie agressief gedrag |
|
Choi, S. H., Park, K. W., Na, D. L., Han, H. J., Kim, E.-J., Shim, Y. S., & Lee, J.-H. (2011). Tolerability and efficacy of memantine add-on therapy to rivastigmine transdermal patches in mild to moderate Alzheimer’s disease: a multicenter, randomized, open-label, parallel-group study. Current Medical Research and Opinion, 27(7), 1375–1383. |
Trial, niet placebo-gecontroleerd. |
|
Cretu, O., Szalontay, A. S., Chirita, R., & Chirita, V. (2008). [Effect of memantine treatment on patients with moderate-to-severe Alzheimer’s disease treated with donepezil]. Revista medico-chirurgicala a Societatii de Medici si Naturalisti din Iasi, 112(3), 641–645. |
Trial, publicatie in Roemeens. |
|
De Deyn, P., Rabheru, K., & Rasmussen, A. (1999). A randomized trial of risperidone, placebo, and haloperidol for behavioral symptoms of dementia. Neurology, (53), 945–956. |
Trial, geen specifieke indicatie agressief gedrag |
|
De Deyn, P., Carrasco, M., Deberdt, W., Jeandel, C., Hay, D., Feldman, P., … Breier, A. (2004). Olanzapine versus placebo in the treatment of psychosis with or without associated behavioral disturbances in patients with Alzheimer’s disease. Int J Geriatr Psychiatry, 19(2), 115–26. |
Trial, geen specifieke indicatie agressief gedrag |
|
De Deyn, P., Jeste, D., Swanink, R., Kostic, D., & Breder, C. (2005). Aripiprazole for the Treatment of Psychosis in Patients With Alzheimer’s Disease. J Clin Psychopharmacol, 25(5), 463–467. |
Trial, geen specifieke indicatie agressief gedrag |
|
Deberdt, W., Dysken, M., Rappaport, S., Feldman, P., Young, C., & Hay, D. (2005). Comparison of Olanzapine and Risperidone in the Treatment of Psychosis and Associated Behavioral Disturbances in Patients With Dementia. Am J Geriatr Psychiatry, 13(August), 722–730. |
Trial, geen specifieke indicatie agressief gedrag |
|
Devanand, D., Sackeim, H. A., Marder, K., Michaels, K., Bell, K., Sullivan, M. A., … Mayeux, R. (1998). A Randomized, Placebo-Controlled Dose-Comparison Trial of Haloperidol for Psychosis and Disruptive Behaviors in Alzheimer’s Disease. American Journal Psychiatry, 155(November), 1512–1520. |
Trial, geen specifieke indicatie agressief gedrag |
|
Dysken, M. W., Sano, M., Asthana, S., Vertrees, J. E., Pallaki, M., Llorente, M., … Guarino, P. D. (2014). Effect of vitamin E and memantine on functional decline in Alzheimer disease: the TEAM-AD VA cooperative randomized trial. JAMA, 311(1), 33–44. |
Trial, geen specifieke indicatie agressief gedrag |
|
Erkinjuntti, T., Kurz, A., Gauthier, S., Bullock, R., Lilienfeld, S., & Damaraju, C. V. (2002). Efficacy of galantamine in probable vascular dementia and Alzheimer’s disease combined with cerebrovascular disease: a randomised trial. Lancet (London, England), 359(9314), 1283–1290. |
Trial, geen specifieke indicatie agressief gedrag |
|
Finkel, S., Lyons, J., Anderson, R., & Sherrell, K. (1995). A Randomized, Placebo-controlled Trial of Thiothixene in Agitated, Demented Nursing Home Patients.International Journal of Geriatric Psychiatry, 10(June 1994), 129–136. |
Trial met middel wat niet verkrijgbaar is in Nederland. |
|
Finkel, S. I., Mintzer, J. E., Dysken, M., Krishnan, K. R., Burt, T., & McRae, T. (2004). A randomized, placebo-controlled study of the efficacy and safety of sertraline in the treatment of the behavioral manifestations of Alzheimer’s disease in outpatients treated with donepezil. Int J Geriatr Psychiatry, 19(1), 9–18. |
Trial, geen specifieke indicatie agressief gedrag |
|
Gaber, S., Ronzoli, S., Bruno, A., & Biagi, A. (2001). Sertraline versus small doses of haloperidol in the treatment of agitated behavior in patients with dementia.Archives of Gerontology and Geriatrics. Supplement, 7, 159–162. Journal Article. |
Trial, niet placebo-gecontroleerd |
|
Gauthier, S., Feldman, H., Hecker, J., Vellas, B., Emir, B., & Subbiah, P. (2002). Functional, cognitive and behavioral effects of donepezil in patients with moderate Alzheimer’s disease. Current Medical Research and Opinion, 18(6), 347–354. |
Trial, geen specifieke indicatie agressief gedrag |
|
Gavrilova, S. I., Preuss, U. W., Wong, J. W. M., Hoerr, R., Kaschel, R., & Bachinskaya, N. (2014). Efficacy and safety of Ginkgo biloba extract EGb 761 in mild cognitive impairment with neuropsychiatric symptoms: a randomized, placebo-controlled, double-blind, multi-center trial. International Journal of Geriatric Psychiatry, 29(10), 1087–1095. |
Trial in populatie van mensen zonder dementie en zonder indicatie agressief gedrag. |
|
Gehrman, P. R., Connor, D. J., Martin, J. L., Shochat, T., Corey-Bloom, J., & Ancoli-Israel, S. (2009). Melatonin fails to improve sleep or agitation in double-blind randomized placebo-controlled trial of institutionalized patients with Alzheimer disease. Am J Geriatr Psychiatry, 17(2), 166–169. |
Trial, geen specifieke indicatie agressief gedrag |
|
Grossberg, G. T., Manes, F., Allegri, R. F., Gutierrez-Robledo, L. M., Gloger, S., Xie, L., … Graham, S. M. (2013). The safety, tolerability, and efficacy of once-daily memantine (28 mg): a multinational, randomized, double-blind, placebo-controlled trial in patients with moderate-to-severe Alzheimer’s disease taking cholinesterase inhibitors. CNS Drugs, 27(6), 469–478. |
Trial, geen specifieke indicatie agressief gedrag |
|
Hamilton, L., & Bennett, J. (1962). The Use Of Trifluoperazine in Geriatric Patients With Chronic Brain Syndrome. J Am Geriatr Soc, Feb(10), 140–147.Herrmann, N., Lanctot, K. L., Rothenburg, L. S., & Eryavec, G. (2007). A placebo-controlled trial of valproate for agitation and aggression in Alzheimer’s disease.Dement Geriatr Cogn Disord, 23(2), 116–119. |
Trial met middel wat niet verkrijgbaar is in Nederland. |
|
Herrmann N, Lanctot KL, Rothenburg LS, Eryavec G. A placebo-controlled trial of valproate for agitation and aggression in Alzheimer’s disease. Dement Geriatr Cogn Disord. 2007;23(2):116-119. |
Trial, geen specifieke indicatie agressief gedrag |
|
Herrschaft, H., Nacu, A., Likhachev, S., Sholomov, I., Hoerr, R., & Schlaefke, S. (2012). Ginkgo biloba extract EGb 761(R) in dementia with neuropsychiatric features: a randomised, placebo-controlled trial to confirm the efficacy and safety of a daily dose of 240 mg. J Psychiatr Res, 46(6), 716–723. |
Trial, geen specifieke indicatie agressief gedrag |
|
Holmes, C., Wilkinson, D., Dean, C., Clare, C., El-Okl, M., Hensford, C., & Moghul, S. (2007, April). Risperidone and rivastigmine and agitated behaviour in severe Alzheimer’s disease: a randomised double blind placebo controlled study. International Journal of Geriatric Psychiatry. |
Trial, niet placebo-gecontroleerd |
|
NCT00260624. (n.d.). Escitalopram Treatment of Patients With Agitated Dementia. Retrieved from https://clinicaltrials.gov/ct2/show/NCT00260624 |
Trial, niet placebo-gecontroleerd |
|
Ihl, R., Bachinskaya, N., Korczyn, A. D., Vakhapova, V., Tribanek, M., Hoerr, R., & Napryeyenko, O. (2011). Efficacy and safety of a once-daily formulation of Ginkgo biloba extract EGb 761 in dementia with neuropsychiatric features: a randomized controlled trial. Int J Geriatr Psychiatry, 26(11), 1186–1194. |
Trial, geen specifieke indicatie agressief gedrag |
|
Ihl, R., Tribanek, M., Bachinskaya, N., & Group, G. S. (2012). Efficacy and tolerability of a once daily formulation of Ginkgo biloba extract EGb 761 in Alzheimer’s disease and vascular dementia: results from a randomised controlled trial. Pharmacopsychiatry, 45(2), 41–46. |
Trial, geen specifieke indicatie agressief gedrag |
|
Katz, I., Jeste, D., Mintzer, J., Clyde, C., Napolitano, J., & Brecher, M. (1999). Comparison of Risperidone and Placebo for Psychosis and Behavioral Disturbances Associated With Dementia: A Randomized, Double-Blind Trial. J Clin Psychiatry, 60(February), 107–115. |
Trial, geen specifieke indicatie agressief gedrag |
|
Kurlan, R., Cummings, J., Raman, R., & Thal, L. (2007). Quetiapine for agitation or psychosis in patients with dementia and parkinsonism. Neurology, 68(17), 1356–63. |
Trial, geen specifieke indicatie agressief gedrag |
|
Lebert, F., Stekke, W., Hasenbroekx, C., & Pasquier, F. (2004). Frontotemporal dementia: a randomised, controlled trial with trazodone. Dement Geriatr Cogn Disord, 17(4), 355–359. |
Trial, geen specifieke indicatie agressief gedrag |
|
Macdonald, A., Briggs, K., Poppe, M., Higgins, A., Velayudhan, L., & Lovestone, S. (2008). A feasibility and tolerability study of lithium in Alzheimer’s disease.International Journal of Geriatric Psychiatry, 23(7), 704–711. |
Trial, geen specifieke indicatie agressief gedrag en niet placebo-gecontroleerd. |
|
Meehan, K. M., Wang, H., David, S. R., Nisivoccia, J. R., Jones, B., Beasley Jr., C. M., … Breier, A. (2002). Comparison of rapidly acting intramuscular olanzapine, lorazepam, and placebo: a double-blind, randomized study in acutely agitated patients with dementia. Neuropsychopharmacology, 26(4), 494–504. |
Trial met middel met intramusculaire toedieningsvorm |
|
Mintzer, J., Greenspan, A., Caers, I., Hove, I., Kushner, S., Weiner, M., … Schneider, L. (2006). Risperidone in the Treatment of Psychosis of Alzheimer Disease: Results From a Prospective Clinical Trial. Am J Geriatr Psychiatry, (March), 280–291. |
Trial, geen specifieke indicatie agressief gedrag |
|
Mintzer, J., Tune, L., Breder, C., Swanink, M., & Marcus, R. (2007). Aripiprazole for the Treatment of Psychoses in Institutionalized Patients With Alzheimer Dementia : A Multicenter , Randomized , of Three Fixed Doses. Am J Geriatr Psychiatry, (November), 918–931. |
Trial, geen specifieke indicatie agressief gedrag |
|
Mizukami, K., Asada, T., Kinoshita, T., Tanaka, K., Sonohara, K., Nakai, R., … Toba, K. (2009). A randomized cross-over study of a traditional Japanese medicine (kampo), yokukansan, in the treatment of the behavioural and psychological symptoms of dementia. The International Journal of Neuropsychopharmacology / Official Scientific Journal of the Collegium Internationale Neuropsychopharmacologicum (CINP), 12(2), 191–199. |
Trial, niet placebo-gecontroleerd. |
|
Napryeyenko, O., & Borzenko, I. (2007). Ginkgo biloba special extract in dementia with neuropsychiatric features. A randomised, placebo-controlled, double-blind clinical trial. Arzneimittel-Forschung, 57(1), 4–11. |
Trial, geen specifieke indicatie agressief gedrag |
|
Nikolova G , Yancheva S , Raychev I, H. R. (2013). Ginkgo biloba extract in dementia: A 22-week randomised, placebo-controlled, double-blind trial . Bulgarian Neurology, 14, 139 – 143. |
Trial, publicatie in Bulgaars. |
|
Nyth, A. L., & Gottfries, C. G. (1990). The clinical efficacy of citalopram in treatment of emotional disturbances in dementia disorders. A Nordic multicentre study. Br J Psychiatry, 157, 894–901. |
Trial, geen specifieke indicatie agressief gedrag |
|
Olafsson, K., Jorgensen, S., Jensen, H. V, Bille, A., Arup, P., & Andersen, J. (1992). Fluvoxamine in the treatment of demented elderly patients: a double-blind, placebo-controlled study. Acta Psychiatrica Scandinavica, 85(6), 453–456. |
Trial, geen specifieke indicatie agressief gedrag |
|
Paleacu, D., Barak, Y., Mirecky, I., & Mazeh, D. (2008). Quetiapine treatment for behavioural and psychological symptoms of dementia in Alzheimer’s disease patients: a 6-week, double-blind, placebo-controlled study. Int J Geriatr Psychiatry, 23(September 2007), 393–400. |
Trial, geen specifieke indicatie agressief gedrag |
|
Petrie, W., Ban, T., Berney, S., Fujimori, M., Guy, W., Ragheb, M., … Schaffer, D. (1982). Loxapine in Psychogeriatrics: A Placebo- and Standard-Controlled Clinical Investigation. Journal Clinical Psychopharmacology, 2(2), 122–126. |
Trial, geen specifieke indicatie agressief gedrag |
|
Pollock, B., Mulsant, B., Rosen, J., Sweet, R., Mazumdar, S., Bharucha, A., … Chew, M. (2002). Comparison of Citalopram, Perphenazine, and Placebo for the Acute Treatment of Psychosis and Behavioral Disturbances in Hospitalized , Demented Patients. Am J Psychiatry, 159(March), 460–465. |
Trial, geen specifieke indicatie agressief gedrag |
|
Pollock, B. G., Mulsant, B. H., Rosen, J., Mazumdar, S., Blakesley, R. E., Houck, P. R., & Huber, K. A. (2007). A double-blind comparison of citalopram and risperidone for the treatment of behavioral and psychotic symptoms associated with dementia. The American Journal of Geriatric Psychiatry : Official Journal of the American Association for Geriatric Psychiatry, 15(11), 942–952. |
Trial, niet placebo-gecontroleerd |
|
Porsteinsson, A. P., Grossberg, G. T., Mintzer, J., & Olin, J. T. (2008). Memantine treatment in patients with mild to moderate Alzheimer’s disease already receiving a cholinesterase inhibitor: a randomized, double-blind, placebo-controlled trial. Current Alzheimer Research, 5(1), 83–89. |
Trial, geen specifieke indicatie agressief gedrag |
|
Profenno, L. A., Jakimovich, L., Holt, C. J., Porsteinsson, A., & Tariot, P. N. (2005). A randomized, double-blind, placebo-controlled pilot trial of safety and tolerability of two doses of divalproex sodium in outpatients with probable Alzheimer’s disease. Curr Alzheimer Res, 2(5), 553–558. |
Trial, geen specifieke indicatie agressief gedrag |
|
Rabey, J. M., Prokhorov, T., Miniovitz, A., Dobronevsky, E., & Klein, C. (2007). Effect of quetiapine in psychotic Parkinson’s disease patients: a double-blind labeled study of 3 months’ duration. Movement Disorders : Official Journal of the Movement Disorder Society, 22(3), 313–318. |
Trial, geen specifieke indicatie agressief gedrag |
|
Rada, R., & Kellner, R. (1976). Thiothixene in the Treatment of Geriatric Patients With Chronic Organic Brain Syndrome. Journal of the American Geriatrics Society, 24(3), 105–107. |
Trial, geen specifieke indicatie agressief gedrag |
|
Reisberg, B., Doody, R., Stoffler, A., Schmitt, F., Ferris, S., & Mobius, H. J. (2003). Memantine in moderate-to-severe Alzheimer’s disease. The New England Journal of Medicine, 348(14), 1333–1341. |
Trial, geen specifieke indicatie agressief gedrag |
|
Riemersma-van der Lek RF, Swaab DF, Twisk J, Hol EM, Hoogendijk WJ, Van Someren EJ. Effect of Bright Light and Melatonin on Cognitive and Noncognitive Function in Elderly Residents of Group Care Facilities. Jama. 2008;299(22):2642. |
Trial, geen specifieke indicatie agressief gedrag |
|
RIS-BEL-14. (1997). Unpublished. |
Trial, geen specifieke indicatie agressief gedrag |
|
Rockwood, K., Mintzer, J., Truyen, L., Wessel, T., & Wilkinson, D. (2001). Effects of a flexible galantamine dose in Alzheimer’s disease: a randomised, controlled trial. Journal of Neurology, Neurosurgery, and Psychiatry, 71(5), 589–595. |
Trial, geen specifieke indicatie agressief gedrag |
|
Satterlee, W. (1995). Olanzapine versus Placebo in the Treatment of Patients with Psychosis Associated with Dementia (F1D-MC-HGAO). Abstract. |
Trial, geen specifieke indicatie agressief gedrag |
|
Schneider, L. S., Tariot, P. N., Lyketsos, C. G., Dagerman, K. S., Davis, K. L., Davis, S., … Lieberman, J. A. (2001). National Institute of Mental Health Clinical Antipsychotic Trials of Intervention Effectiveness (CATIE): Alzheimer disease trial methodology. The American Journal of Geriatric Psychiatry : Official Journal of the American Association for Geriatric Psychiatry, 9(4), 346–360. |
Design van een trial. |
|
Schneider, L. S., Katz, I. R., Park, S., Napolitano, J., Martinez, R. A., & Azen, S. P. (2003). Psychosis of Alzheimer disease: validity of the construct and response to risperidone. The American Journal of Geriatric Psychiatry : Official Journal of the American Association for Geriatric Psychiatry,11(4), 414–425. |
Trial, geen specifieke indicatie agressief gedrag |
|
Schneider, L. S., Tariot, P. N., Dagerman, K. S., Davis, S. M., Hsiao, J. K., Ismail, M. S., … Lieberman, J. A. (2006). Effectiveness of atypical antipsychotic drugs in patients with Alzheimer’s disease. N Engl J Med, 355(15), 1525–1538. |
Trial, geen specifieke indicatie agressief gedrag |
|
Serfaty, M., Kennell-Webb, S., Warner, J., Blizard, R., & Raven, P. (2002). Double blind randomised placebo controlled trial of low dose melatonin for sleep disorders in dementia. Int J Geriatr Psychiatry, 17(12), 1120–1127. |
Trial, geen specifieke indicatie agressief gedrag |
|
Siddique, H., Hynan, L. S., & Weiner, M. F. (2009). Effect of a serotonin reuptake inhibitor on irritability, apathy, and psychotic symptoms in patients with Alzheimer’s disease. J Clin Psychiatry, 70(6), 915–918. |
Trial, niet placebo-gecontroleerd |
|
Singer, C., Tractenberg, R. E., Kaye, J., Schafer, K., Gamst, A., Grundman, M., … Thal, L. J. (2003). A multicenter, placebo-controlled trial of melatonin for sleep disturbance in Alzheimer’s disease. Sleep, 26(7), 893–901. |
Trial, geen specifieke indicatie agressief gedrag |
|
Sival, R. C., Haffmans, P. M., Jansen, P. A., Duursma, S. A., & Eikelenboom, P. (2002). Sodium valproate in the treatment of aggressive behavior in patients with dementia--a randomized placebo controlled clinical trial. Int J Geriatr Psychiatry, 17(6), 579–585. |
Trial met design zonder parallelle groepen/ patiënten vormen hun eigen controles. |
|
Street, J. S., Clark, W. S., Gannon, K. S., Cummings, J. L., Bymaster, F. P., Tamura, R. N., … Breier, A. (2000). Olanzapine treatment of psychotic and behavioral symptoms in patients with Alzheimer disease in nursing care facilities: a double-blind, randomized, placebo-controlled trial. The HGEU Study Group. Arch Gen Psychiatry, 57(10), 968–976. |
Trial, geen specifieke indicatie agressief gedrag |
|
Streim, J., Porsteinsson, A., Breder, C., Swanink, R., & Marcus, R. (2008). Placebo-Controlled Study of Aripiprazole for the Treatment of Psychosis in Nursing Home Patients with Alzheimer Disease. Am J Geriatr Psychiatry, (July), 537–550. |
Trial, geen specifieke indicatie agressief gedrag |
|
Sugerman, A., Williams, B., & Alderstein, A. (1964). Haloperidol in the psychiatric disorders of old age. Clinical Notes, 1190–1192. |
Trial, geen specifieke indicatie agressief gedrag |
|
Sultzer, D. L., Gray, K. F., Gunay, I., Berisford, M. A., & Mahler, M. E. (1997). A double-blind comparison of trazodone and haloperidol for treatment of agitation in patients with dementia. The American Journal of Geriatric Psychiatry : Official Journal of the American Association for Geriatric Psychiatry, 5(1), 60–69. |
Trial, niet placebo-gecontroleerd |
|
Sultzer, D. L., Davis, S. M., Tariot, P. N., Dagerman, K. S., Lebowitz, B. D., Lyketsos, C. G., … Schneider, L. S. (2008). Clinical symptom responses to atypical antipsychotic medications in Alzheimer’s disease: phase 1 outcomes from the CATIE-AD effectiveness trial. Am J Psychiatry, 165(7), 844–854. |
Trial, geen specifieke indicatie agressief gedrag |
|
Tariot, P. N., Cummings, J. L., Katz, I. R., Mintzer, J., Perdomo, C. A., Schwam, E. M., & Whalen, E. (2001). A randomized, double-blind, placebo-controlled study of the efficacy and safety of donepezil in patients with Alzheimer’s disease in the nursing home setting. Journal of the American Geriatrics Society, 49(12), 1590–1599. |
Trial, geen specifieke indicatie agressief gedrag |
|
Tariot, P. N., Farlow, M. R., Grossberg, G. T., Graham, S. M., McDonald, S., & Gergel, I. (2004). Memantine treatment in patients with moderate to severe Alzheimer disease already receiving donepezil: a randomized controlled trial. JAMA, 291(3), 317–324. |
Trial, geen specifieke indicatie agressief gedrag |
|
Tariot, P., Schneider, L., Katz, I., Mintzer, J., Street, J., Copenhaver, M., & Williams-Hughes, C. (2006). Quetiapine Treatment of Psychosis Associated With Dementia : A Double-Blind , Randomized , Placebo-Controlled Clinical Trial. Am J Geriatr Psychiatry, 14(9), 767–776. |
Trial, geen specifieke indicatie agressief gedrag |
|
Tariot, P. N., Schneider, L. S., Cummings, J., Thomas, R. G., Raman, R., Jakimovich, L. J., … Aisen, P. S. (2011). Chronic divalproex sodium to attenuate agitation and clinical progression of Alzheimer disease. Arch Gen Psychiatry, 68(8), 853–861. |
Trial, geen specifieke indicatie agressief gedrag |
|
van den Elsen, G. A. H., Ahmed, A. I. A., Verkes, R.-J., Feuth, T., van der Marck, M. A., & Olde Rikkert, M. G. M. (2015). Tetrahydrocannabinol in Behavioral Disturbances in Dementia: A Crossover Randomized Controlled Trial. The American Journal of Geriatric Psychiatry : Official Journal of the American Association for Geriatric Psychiatry, 23(12), 1214–1224. |
Trial, geen specifieke indicatie agressief gedrag |
|
van den Elsen, G. A. H., Ahmed, A. I. A., Verkes, R.-J. J., Kramers, C., Feuth, T., Rosenberg, P. B., … Olde Rikkert, M. G. M. (2015). Tetrahydrocannabinol for neuropsychiatric symptoms in dementia: A randomized controlled trial. Neurology, 84(23), 2338–2346. |
Trial, geen specifieke indicatie agressief gedrag |
|
van Dyck, C. H., Tariot, P. N., Meyers, B., & Malca Resnick, E. (2007). A 24-week randomized, controlled trial of memantine in patients with moderate-to-severe Alzheimer disease. Alzheimer Disease and Associated Disorders, 21(2), 136–143. |
Trial, geen specifieke indicatie agressief gedrag |
|
Walther, S., Schupbach, B., Seifritz, E., Homan, P., & Strik, W. (2011, April). Randomized, controlled crossover trial of dronabinol, 2.5 mg, for agitation in 2 patients with dementia. Journal of Clinical Psychopharmacology. |
RCT met n=2. |
|
Winblad, B., Engedal, K., Soininen, H., Verhey, F., Waldemar, G., Wimo, A., … Subbiah, P. (2001). A 1-year, randomized, placebo-controlled study of donepezil in patients with mild to moderate AD. Neurology, 57(3), 489–495. |
Trial, geen specifieke indicatie agressief gedrag |
|
Zheng, L., Mack, W. J., Dagerman, K. S., Hsiao, J. K., Lebowitz, B. D., Lyketsos, C. G., … Schneider, L. S. (2009). Metabolic changes associated with second-generation antipsychotic use in Alzheimer’s disease patients: the CATIE-AD study. Am J Psychiatry, 166(5), 583–590. |
Trial, geen specifieke indicatie agressief gedrag |
|
Systematische reviews |
|
|
Ballard, C., Waite, J., & Birks, J. (2006). Atypical antipsychotics for aggression and psychosis in Alzheimer ’ s disease (Review). The Cochrane Library, (1), 1–135. |
Meta-analyse van trials die niet voldoen aan criteria. |
|
Bolea-Alamanac, B. M., Davies, S. J., Christmas, D. M., Baxter, H., Cullum, S., & Nutt, D. J. (2011). Cyproterone to treat aggressivity in dementia: a clinical case and systematic review. J Psychopharmacol, 25(1), 141–145. |
Systematische review waarbij geen placebo-gecontroleerde trials werden gevonden. |
|
Carson, S., McDonagh, M., & Peterson, K. (2006). A systematic review of the efficacy and safety of atypical antipsychotics in patients with psychological and behavioral symptoms of dementia. Journal of the American Geriatrics Society, 54(2), 354–361. |
Meta-analyse maar niet met alle trials die voldoen aan criteria |
|
Cheung, G., & Stapelberg, J. (2011). Quetiapine for the treatment of behavioural and psychological symptoms of dementia (BPSD): a meta-analysis of randomised placebo-controlled trials. The New Zealand Medical Journal, 124(1336), 39–50. |
Meta-analyse van trials die niet voldoen aan criteria. |
|
geen auteurs. Treatment of Parkinson’s disease. Psychological disorders: striking a balance in order to optimise antiparkinsonian treatment. (2011). Prescrire Int, 20(120), 242–245. |
Meta-analyse in populatie met ziekte van Parkinson, zonder dementie. |
|
Jansen, S. L., Forbes, D. A., Duncan, V., & Morgan, D. G. (2006). Melatonin for cognitive impairment. Cochrane Database Syst Rev, (1), Cd003802. |
Meta-analyse van trials die niet voldoen aan criteria. |
|
Jansen, S. L., Forbes, D., Duncan, V., Morgan, D. G., & Malouf, R. (2006). Melatonin for the treatment of dementia. Cochrane Database of Systematic Reviews, 3(4). |
Meta-analyse van trials die niet voldoen aan criteria. |
|
Kavanagh, S., Gaudig, M., Van Baelen, B., Adami, M., Delgado, A., Guzman, C., … Schauble, B. (2011). Galantamine and behavior in Alzheimer disease: analysis of four trials. Acta Neurol Scand, 124(5), 302–308. |
Meta-analyse van trials zonder specifieke indicatie agressief gedrag. |
|
Krishnan, S., Cairns, R., & Howard, R. (2009). Cannabinoids for the treatment of dementia. Cochrane Database Syst Rev, (2), Cd007204. |
Review van trials zonder specifieke indicatie agressief gedrag. |
|
Lee, P., Gill, S., Freedman, M., Bronskill, S., Hillmer, M., & Rochon, P. (2004). Atypical antipsychotic drugs in the treatment of behavioural and psychological symptoms of dementia: systematic review. BMJ, 329, 1–5. |
Meta-analyse maar niet met alle trials die voldoen aan criteria |
|
Lockhart, I. A. A., Orme, M. E. E., & Mitchell, S. A. A. (2011). The efficacy of licensed-indication use of donepezil and memantine monotherapies for treating behavioural and psychological symptoms of dementia in patients with Alzheimer’s disease: systematic review and meta-analysis. Dement Geriatr Cogn Dis Extra, 1(1), 212–227. |
Meta-analyse van trials zonder specifieke indicatie agressief gedrag. |
|
Lonergan, E., & Luxenberg, J. (2009). Valproate preparations for agitation in dementia. Cochrane Database Syst Rev, (3), Cd003945. |
Meta-analyse met te weinig gelijkenis in inclusie van trials. |
|
Lonergan, E., Luxenberg, J., Colford, J., & Birks, J. (2010). Haloperidol for agitation in dementia (Review). The Cochrane Library, (12), 1–42. |
Meta-analyse van trials die niet voldoen aan criteria. |
|
Ma, H., Huang, Y., Cong, Z., Wang, Y., Jiang, W., Gao, S., & Zhu, G. (2014). The Efficacy and Safety of Atypical Antipsychotics for the Treatment of Dementia: A Meta-Analysis of Randomized Placebo-Controlled Trials. Journal of Alzheimer’s Disease, 42, 915–937. |
Meta-analyse van trials die niet voldoen aan criteria. |
|
Maher, A., Maglione, M., Bagley, S., Suttorp, M., Hu, J., Ewing, B., … Sultzer, D. (2011). Efficacy and Comparative Effectiveness of Atypical Antipsychotic Medications for Off-Label Uses in Adults. Journal of the American Medical Association, 306(12), 1359–1370. |
Meta-analyse van trials die niet voldoen aan criteria. |
|
Martinon-Torres, G., Fioravanti, M., & Grimley, E. J. (2004). Trazodone for agitation in dementia. Cochrane Database Syst Rev, (4), Cd004990. |
Review zonder meta-analyses. |
|
Matsuda, Y., Kishi, T., Shibayama, H., & Iwata, N. (2013). Yokukansan in the treatment of behavioral and psychological symptoms of dementia: a systematic review and meta-analysis of randomized controlled trials. Human Psychopharmacology, 28(1), 80–86. |
Meta-analyse van niet-placebogecontroleerde trials. |
|
Matsunaga, S., Kishi, T., & Iwata, N. (2015). Combination therapy with cholinesterase inhibitors and memantine for Alzheimer’s disease: a systematic review and meta-analysis. Int J Neuropsychopharmacol, 18(5). |
Meta-analyse van trials zonder specifieke indicatie agressief gedrag. |
|
Seitz, D. P., Adunuri, N., Gill, S. S., Gruneir, A., Herrmann, N., & Rochon, P. (2011). Antidepressants for agitation and psychosis in dementia. Cochrane Database Syst Rev, (2), Cd008191.
|
Meta-analyse van antidepressiva, maar niet versus placebo op agitatie. |
|
Seitz, D. P., Gill, S. S., Herrmann, N., Brisbin, S., Rapoport, M. J., Rines, J., … Conn, D. K. (2013). Pharmacological treatments for neuropsychiatric symptoms of dementia in long-term care: a systematic review. Int Psychogeriatr, 25(2), 185–203. |
Review met daarin meta-analyses, maar niet van trials met specifieke indicatie agitatie. |
|
Stinton, C., McKeith, I., Taylor, J. P., Lafortune, L., Mioshi, E., Mak, E., … O’Brien, J. T. (2015). Pharmacological Management of Lewy Body Dementia: A Systematic Review and Meta-Analysis. Am J Psychiatry, 172(8), 731–742. |
Meta-analyse van trials die niet aan onze criteria voldoen (meeste niet placebo-gecontroleerd of geen specifieke indicatie agitatie). |
|
Tampi, R., Aziz, R., Kantrowitz, J., Wilkins, K. M., Zdanys, K., & Muralee, S. (2009). Carbamazepine and oxcarbazepine for the treatment of behavioural and psychological symptoms of dementia (BPSD). Cochrane Database of Systematic Reviews. CD007761 |
Protocol van review. |
|
Tan, M. S., Yu, J. T., Tan, C. C., Wang, H. F., Meng, X. F., Wang, C., … Tan, L. (2015). Efficacy and adverse effects of ginkgo biloba for cognitive impairment and dementia: a systematic review and meta-analysis. J Alzheimers Dis, 43(2), 589–603. |
Meta-analyse van trials zonder specifieke indicatie agressief gedrag. |
|
von Gunten, A., Schlaefke, S., & Uberla, K. (2015). Efficacy of Ginkgo biloba extract EGb 761 in dementia with behavioural and psychological symptoms: A systematic review. The World Journal of Biological Psychiatry : The Official Journal of the World Federation of Societies of Biological Psychiatry, 1–12. |
Meta-analyse van trials zonder specifieke indicatie agressief gedrag. |
|
Wang, J., Yu, J. T., Wang, H. F., Meng, X. F., Wang, C., Tan, C. C., & Tan, L. (2015). Pharmacological treatment of neuropsychiatric symptoms in Alzheimer’s disease: a systematic review and meta-analysis. J Neurol Neurosurg Psychiatry, 86(1), 101–109. |
Meta-analyse van trials zonder specifieke indicatie agressief gedrag. |
|
Xiao, H., Su, Y., Cao, X., Sun, S., & Liang, Z. (2010). A meta-analysis of mood stabilizers for Alzheimer’s disease. J Huazhong Univ Sci Technolog Med Sci, 30(5), 652–658. |
Meta-analyse met te weinig gelijkenis in inclusie van trials. |
Bijlage 3.2 Risico op bias van RCT’s naar psychofarmaca voor geagiteerd gedrag bij mensen met dementie
|
|
1. randomisa-tieproces |
2. afwijkingen van beoogde interventie |
3. ontbrekende uitkomsten |
4. uitkomst-metingen |
5. selectieve rapportage |
6. overig |
totaal aantal items zonder bias |
|
Klasieke antipsychotica |
|||||||
|
Allain 2000 |
geen bias |
onduidelijk |
wel bias |
onduidelijk |
geen bias |
wel bias |
2 |
|
Auchus 1997 |
wel bias |
onduidelijk |
onduidelijk |
onduidelijk |
geen bias |
wel bias |
1 |
|
Teri 2000 |
onduidelijk |
onduidelijk |
geen bias |
geen bias |
geen bias |
geen bias |
4 |
|
Atypische antipsychotica |
|||||||
|
Zhong 2007 |
wel bias |
onduidelijk |
wel bias |
geen bias |
wel bias |
wel bias |
1 |
|
Ballard 2005 |
onduidelijk |
onduidelijk |
wel bias |
geen bias |
wel bias |
wel bias |
1 |
|
Allain 2000 |
onduidelijk |
onduidelijk |
onduidelijk |
onduidelijk |
geen bias |
wel bias |
1 |
|
Brodaty 2003 |
wel bias |
onduidelijk |
wel bias |
onduidelijk |
wel bias |
wel bias |
0 |
|
Anti-depressiva |
|||||||
|
Porsteinsson 2014* |
wel bias |
geen bias |
onduidelijk |
geen bias |
wel bias |
geen bias |
3 |
|
Teri 2000 |
geen bias |
onduidelijk |
geen bias |
geen bias |
geen bias |
wel bias |
4 |
|
Auchus 1997 |
wel bias |
onduidelijk |
wel bias |
onduidelijk |
onduidelijk |
geen bias |
1 |
|
Anti-epileptica |
|||||||
|
Olin 2001 |
onduidelijk |
onduidelijk |
geen bias |
onduidelijk |
onduidelijk |
wel bias |
1 |
|
Tariot 1998 |
onduidelijk |
geen bias |
geen bias |
geen bias |
onduidelijk |
wel bias |
3 |
|
Sommer 2009 |
onduidelijk |
geen bias |
geen bias |
geen bias |
geen bias |
wel bias |
4 |
|
Tariot 2005 |
onduidelijk |
geen bias |
geen bias |
geen bias |
onduidelijk |
wel bias |
3 |
|
Porsteinsson 2001 |
wel bias |
geen bias |
geen bias |
geen bias |
onduidelijk |
wel bias |
3 |
|
Anti-dementie middelen |
|||||||
|
Howard 2007 (CALM-AD) |
onduidelijk |
onduidelijk |
wel bias |
geen bias |
geen bias |
wel bias |
2 |
|
Burns 2011 |
onduidelijk |
onduidelijk |
wel bias |
geen bias |
geen bias |
wel bias |
2 |
|
Herrmann 2013 |
wel bias |
onduidelijk |
wel bias |
geen bias |
geen bias |
wel bias |
2 |
|
Fox 2012 |
geen bias |
geen bias |
wel bias |
geen bias |
geen bias |
wel bias |
4 |
|
Ballard 2005 |
onduidelijk |
onduidelijk |
wel bias |
geen bias |
geen bias |
wel bias |
2 |
* En andere artikelen over CitAD: newell 2016, Drye 2014, Drye 2012
Bijlage 3.3. Forest plots van RCT’s naar psychofarmaca voor geagiteerd gedrag bij mensen met dementie